题目内容
7.某铁的氧化物(FexO)1.52g溶于足量盐酸中,向所得溶液中通入标准状况下112ml Cl2,恰好将Fe2+完全氧化.x值为( )| A. | 0.80 | B. | 0.85 | C. | 0.90 | D. | 0.93 |
分析 根据电子守恒可知,FexO被氧化为Fe3+转移的电子数和Cl2转移的电子数相等.
解答 解:FexO中Fe的平均化合价为+$\frac{2}{x}$,被氧化为Fe3+,根据电子守恒可知,转移的电子数和Cl2转移的电子数相等.标准状况下112mL Cl2转移电子数为$\frac{0.112L}{22.4L/mol}$×2=0.01mol.则有:$\frac{1.52g}{(56x+16)g/mol}$×(3-$\frac{2}{x}$)×x=0.01mol,解得x=0.8,
故选:A.
点评 本题考查氧化还原反应计算,注意氧化还原反应计算中电子转移守恒运用,本题中注意平均化合价的应用,侧重考查学生的分析计算能力.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
17.设NA代表阿伏加德罗常数,下列说法不正确的是( )
| A. | 1.7gH2O2中含有的电子总数为0.9NA | |
| B. | 92g NO2和N2O4的混合气中含有的氮原子数为2NA | |
| C. | 标准状况下,28 g CO与22.4 L O2所含原子数相等 | |
| D. | 1 mol FeCl3完全水解转化为氢氧化铁胶体后生成NA个胶粒 |
2.下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是( )
| A. | 氧化镁中混有氧化铝 | B. | 氯化铝溶液中混有氯化铁 | ||
| C. | 氧化铁中混有二氧化硅 | D. | 氯化亚铁溶液中混有氯化铜 |
2.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品,用如图中的实验装置进行实验,证明过氧化钠可作供氧剂.
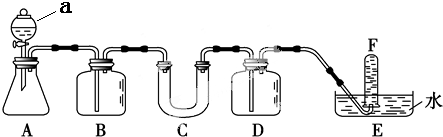
(1)写出仪器a的名称分液漏斗.
(2)A是实验室制取CO2的装置.写出A中发生反应的离子方程式:CaCO3+2H+═CO2↑+H2O+Ca2+.
(3)填写表中空格:
(4)写出仪器C中主要反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
(5)若将钠和过氧化钠的混合物12.4g与足量的水反应后,生成的气体在电火花用下恰好完全反应,且所得溶液的体积为100mL,则所得溶液的物质的量浓度是4mol•L-1.

(1)写出仪器a的名称分液漏斗.
(2)A是实验室制取CO2的装置.写出A中发生反应的离子方程式:CaCO3+2H+═CO2↑+H2O+Ca2+.
(3)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和碳酸氢钠溶液 | |
| D |
(5)若将钠和过氧化钠的混合物12.4g与足量的水反应后,生成的气体在电火花用下恰好完全反应,且所得溶液的体积为100mL,则所得溶液的物质的量浓度是4mol•L-1.
20.关于硅及其化合物的叙述中,正确的是( )
| A. | 硅是良好的半导体材料,且是制造光缆的主要材料 | |
| B. | SiO2不溶于水,也不溶于任何酸 | |
| C. | 可以用焦炭还原二氧化硅生产硅:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| D. | 硅胶可用作催化剂的载体和袋装食品的干燥剂 |
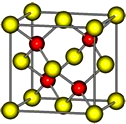 有A、B、C、D、E五种前四周期的元素.A原子核外有1个未成对电子,A+比B原子少一个电子层,B原子得一个电子填入3p轨道后,3p轨道呈全充满状态.C原子的2p轨道有2个未成对电子,D的最高化合价和最低化合价的代数和为4,与C的核电荷数相差8.E位于周期表第12纵列且是六种元素中原子序数最大的.R是由D、E形成的化合物,其晶胞结构如图所示.请回答下列问题:
有A、B、C、D、E五种前四周期的元素.A原子核外有1个未成对电子,A+比B原子少一个电子层,B原子得一个电子填入3p轨道后,3p轨道呈全充满状态.C原子的2p轨道有2个未成对电子,D的最高化合价和最低化合价的代数和为4,与C的核电荷数相差8.E位于周期表第12纵列且是六种元素中原子序数最大的.R是由D、E形成的化合物,其晶胞结构如图所示.请回答下列问题: .
.
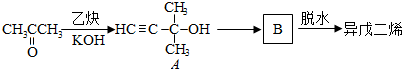
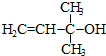 .
. 的合成路线.
的合成路线.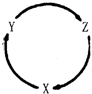 下表各组物质中,满足右图物质一步转化关系的选项是( )
下表各组物质中,满足右图物质一步转化关系的选项是( )