题目内容
写出实验室用KClO3制氧气的化学方程式: ,
(1)从该反应可以看出 mol的KClO3反应可生成 mol O2 molKCl
(2)所以0.4molKClO3 完全反应可生成 mol KCl g O2.
(1)从该反应可以看出
(2)所以0.4molKClO3 完全反应可生成
考点:化学方程式的有关计算
专题:计算题
分析:氯酸钾在二氧化锰的催化作用下受热分解的化学方程式为:2KClO3
2KCl+3O2↑,方程式中各物质的化学计量数之比等于其物质的量之比,根据m=nM计算氧气质量,据此解答.
| ||
| △ |
解答:
解:氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾与氧气,反应化学方程式为:2KClO3
2KCl+3O2↑;
(1)方程式中各物质的化学计量数之比等于其物质的量之比,故2mol的KClO3反应可生成3mol O2、2molKCl;
(2)2KClO3
2KCl+3O2↑
2 2 3
0.4mol n(KCl) n(O2)
故n(KCl)=
=0.4mol
n(O2)=
=0.6mol,m(O2)=0.6mol×32g/mol=19.2g,
故答案为:2KClO3
2KCl+3O2↑;
(1)2;3;2;
(2)0.4;19.2.
| ||
| △ |
(1)方程式中各物质的化学计量数之比等于其物质的量之比,故2mol的KClO3反应可生成3mol O2、2molKCl;
(2)2KClO3
| ||
| △ |
2 2 3
0.4mol n(KCl) n(O2)
故n(KCl)=
| 0.4mol×2 |
| 2 |
n(O2)=
| 0.4mol×3 |
| 2 |
故答案为:2KClO3
| ||
| △ |
(1)2;3;2;
(2)0.4;19.2.
点评:本题考查化学方程式计算及意义,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
 在某晶体中,与某一种微粒X距离最近且等距离的另一种微粒Y 所围成的空间构型为正八面体(如图).该晶体可能是( )
在某晶体中,与某一种微粒X距离最近且等距离的另一种微粒Y 所围成的空间构型为正八面体(如图).该晶体可能是( )| A、NaCl |
| B、CsCl |
| C、CO2 |
下列溶液中的离子能大量共存的是( )
| A、Na+、K+、OH-、SO42- |
| B、Na+、Ba2+、OH-、SO42- |
| C、Na+、Mg2+、SO42-、OH- |
| D、Ca2+、SO42-、NO3-、CO32- |
下列反应生成的新化合物中,不稳定的是( )
| A、SO3与水 |
| B、SO2与水 |
| C、SO2与氯水 |
| D、SO3与NaOH溶液 |
某元素的最高价含氧酸的化学式为HnXO2n,则X元素的气态氢化物的化学式为( )
| A、XH8-3n |
| B、HX |
| C、XH2n |
| D、HnX |
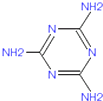 2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺.三聚氰胺(英文名Melamine),是一种三嗪类含氮杂环有机化合物,重要的氮杂环有机化工原料.它的结构简式如图,下列说法中不正确的是( )
2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺.三聚氰胺(英文名Melamine),是一种三嗪类含氮杂环有机化合物,重要的氮杂环有机化工原料.它的结构简式如图,下列说法中不正确的是( )| A、该物质易溶于热水 |
| B、三聚氰胺的分子式为C3N6H6 |
| C、三聚氰胺属于氨基酸的一种 |
| D、三聚氰胺含氮量很高(66%),因此它能冒充蛋白质 |
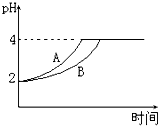 (1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是
(1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是