题目内容
5.短周期元素X、Y、Z、W在元素周期表中的位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,则下列说法正确的是( )| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | Y与氢元素形成的两种常见化合物均为分子晶体 | |
| D. | 四种元素的单质中,W单质的溶沸点最高 |
分析 X、Y、Z、W均为短周期元素,根据元素在周期表中的位置知,X、Y为第二周期元素,Z和W属于第三周期元素,Y原子的最外层电子数是内层电子数的3倍,则Y是O元素,根据其位置知X是N元素、Z是S元素、W是Cl元素,结合元素周期律及物质的性质来解答.
解答 解:X、Y、Z、W均为短周期元素,根据元素在周期表中的位置知,X、Y为第二周期元素,Z和W属于第三周期元素,Y原子的最外层电子数是内层电子数的3倍,则Y是O元素,根据其位置知X是N元素、Z是S元素、W是Cl元素,
A.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径大小顺序为:Z>W>X>Y,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性W>Z,所以其最高价氧化物的水化物酸性:W>Z,故B错误;
C.Y为氧元素,与氢元素形成两种化合物为水、过氧化氢,均由分子构成,均为分子晶体,故C正确;
D.四种元素对应的单质中,常温下S为固体,而其它3种都是气体,所以Z(S元素)对应的单质沸点最高,故D错误;
故选C.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素化合物知识为解答的关键,侧重分析与应用的考查,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
15.电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO${\;}_{3}^{-}$的原理如图所示,下列说法不正确的是( )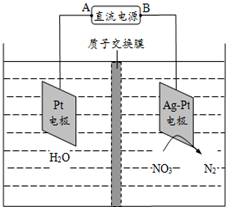

| A. | 铅蓄电池的A极为正极,电极材料为PbO2 | |
| B. | 该电解池的阴极反应式为:2NO3-+12H++10e-═N2↑+6H2O | |
| C. | 该电解池的总反应方程式为:2H2O+4NO3-$\frac{\underline{\;电解\;}}{\;}$2N2↑+5O2↑+4OH- | |
| D. | 若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g |
13.下列变化中,需加氧化剂才能实现的是( )
| A. | H2O→H2 | B. | FeCl3→FeCl2 | C. | C→CO2 | D. | CaO→Ca(OH)2 |
20.下列说法不正确的是( )
| A. | 干燥的氯气能使湿润的有色布条褪色 | |
| B. | 影响气体体积大小的主要因素是微粒间的距离与微粒的大小 | |
| C. | 汤姆生发现原子中存在电子,并提出了“葡萄干面包式”原子结构模型 | |
| D. | 干冰升华的过程只需克服分子间作用力 |
17.实验是化学研究的基础,关于各实验装置图的叙述中,正确的是( )

| A. | 装置①可用干石油的分馏 | |
| B. | 装置②可用于酒精提取溴水中的Br2 | |
| C. | 装置③可用于吸收HCl气体,并能防止倒吸 | |
| D. | 装置④验证乙烯的生成 |
15.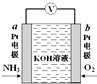 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )| A. | 溶液中OH-向电极a移动 | |
| B. | 负极的电极反应式为:2NH3-6e-+6OH-═N2↑+6H2O | |
| C. | O2在电极b上发生还原反应 | |
| D. | 反应消耗的NH3与O2的物质的量之比为4:5 |

 .
.