题目内容
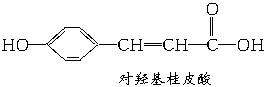
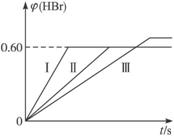
将1 mol Br2(g)和2 mol H2(g)置于某Br2(g)+H2(g) ![]() 2HBr(g);ΔH<0。30 s后达到平衡,其中HBr的体积分数φ(HBr)随时间变化如下图曲线(Ⅱ)所示。
2HBr(g);ΔH<0。30 s后达到平衡,其中HBr的体积分数φ(HBr)随时间变化如下图曲线(Ⅱ)所示。
(1)达平衡时,用Br2(g)表示的化学反应速率是_____________。
(2)若改变反应条件,在甲条件下φ(HBr)的变化如图中曲线(Ⅰ)所示,在乙条件下φ(HBr)的变化如图中曲线(Ⅲ)所示,则甲条件可能是(填入下列条件的序号,下同)___________,乙条件可能是___________。
A.恒温条件下,缩小反应容器体积
B.恒温条件下,扩大反应容器体积
C.恒容条件下,升高温度
D.恒容条件下,降低温度
E.恒温、恒容条件下,加入适当催化剂
F.恒温、恒容时充入氩气
(3)若保持温度不变,在另一相同的
(1)0.015 mol·L-1·s-1 (2)AE D (3)2b-
解析: Br2(g)+H2(g)![]() 2HBr(g)
2HBr(g)
初始: 1 mol 2 mol 0
Δn: 0.9 mol 0.9 mol 1.8 mol
平衡: 0.1 mol 1.1 mol 1.8 mol
(1)v〔Br2(g)〕=![]() =0.015 mol·L-1·s-1
=0.015 mol·L-1·s-1
(2)甲条件下,达到平衡时φ(HBr)不变,平衡状态没有发生改变;达到平衡时所用时间减少,反应速率加快,A、E符合题意.
乙条件下,达到平衡时φ(HBr)增大,平衡向正方向移动;达到平衡时所用时间增长,反应速率减慢,只有D符合题意.
(3)考查等效平衡问题,由于该反应前后气体体积不变,所以只需要“物料比相等”即可,即![]() ,解得:c=2b
,解得:c=2b