题目内容
如图是空气氧化Fe2+转化为Fe3+过程中的实验结果,下列有关说法正确的是( )


| A、使用5% H2SO4氧化效果一定比5% HCl好 |
| B、实验过程最佳氧化条件一定是80℃、5%HCl氧化4小时左右 |
| C、50℃时,图中H2SO4比HCl中氢离子浓度大,所以氧化率高 |
| D、该反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O |
考点:铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:盐酸是一元强酸,硫酸是二元强酸,由图象知,当pH值、其它条件相同温度不同时,温度越高Fe2+的氧化率越大;当温度和其它条件相同,PH值不同时,pH值越大,Fe2+的氧化率越小,在酸性条件下,Fe2+和氧气、氢离子反应生成Fe3+和H2O,注意电荷守恒和得失电子守恒.
解答:
解:A、从图中看出使用5% H2SO4和5% HCl,最终亚铁离子转化率相同,并且反应速率还回受温度的影响,故A错误;
B.从图中看出,实验过程最佳氧化条件一定是80℃、5%HCl氧化3小时左右,故B错误;
C.8h后,H2SO4和HCl亚铁离子氧化率相同,并且阴离子也会对氧化反应产生影响,故C错误;
D.亚铁离子被氧气氧化的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,故D正确.
故选D.
B.从图中看出,实验过程最佳氧化条件一定是80℃、5%HCl氧化3小时左右,故B错误;
C.8h后,H2SO4和HCl亚铁离子氧化率相同,并且阴离子也会对氧化反应产生影响,故C错误;
D.亚铁离子被氧气氧化的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,故D正确.
故选D.
点评:本题考查了外界条件对Fe2+氧化率的影响,难度不大,注意比较氧化率时,要其它条件相同只有一个条件不同才能比较,否则无法得出结论

练习册系列答案
相关题目
下列粒子中,与H3O+所含质子数、电子数相等,且化学键类型相同的粒子是( )
| A、Na+ |
| B、NH4+ |
| C、Ne |
| D、NH3 |
已知:Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反,I2的氧化性比S强.在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是( )
| A、Fe2S3和 Al(OH)3 |
| B、Fe(OH)3和Al(OH)3 |
| C、FeS、Al(OH)3 和S |
| D、Al2S3、FeS和S |
下列物质中不属于羧酸类有机物的是( )
A、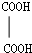 (乙二酸) (乙二酸) |
B、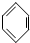 -COOH (苯甲酸) -COOH (苯甲酸) |
| C、CH2CH-COOH(丙烯酸) |
D、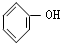 (石炭酸) (石炭酸) |
对于0.1mol/L的醋酸水溶液,下列说法中错误的是( )
| A、加入少量醋酸钠固体,则醋酸根离子浓度减少 |
| B、若加入少量冰醋酸,则氢离子浓度增大 |
| C、若加入少量的NaOH,则醋酸根离子浓度增大 |
| D、若加入少量的盐酸,则醋酸根离子浓度减少 |
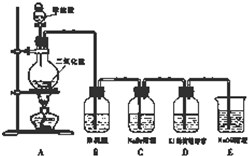 某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)
某校研究性学习小组设计实验,制取氯气以探究Cl2、Br2、I2的氧化性强弱(制取氯气的化学方程式为:MnO2+4HCl(浓)