题目内容
14.将下列铁的化合物溶于盐酸,滴加KSCN溶液后颜色变化最不明显的是( )| A. | FeO | B. | Fe3O4 | C. | Fe2O3 | D. | Fe(OH)3 |
分析 四氧化三铁、氧化铁和氢氧化铁与盐酸反应都会生成铁离子,铁离子与硫氰化钾显示红色,而氧化亚铁与盐酸反应生成亚铁离子,亚铁离子不与硫氰化钾反应,据此进行解答.
解答 解:A.FeO与盐酸反应生成氯化亚铁,滴加KSCN溶液后溶液颜色基本不变,故A正确;
B.Fe3O4与盐酸反应生成氯化亚铁和氯化铁,溶液中含有铁离子,滴加KSCN溶液后溶液变为红色,溶液颜色变化明显,故B错误;
C.Fe2O3与盐酸反应生成氯化铁,溶液中含有铁离子,滴加KSCN溶液后溶液变为红色,溶液颜色变化明显,故C错误;
D.Fe(OH)3与盐酸反应生成氯化亚铁和氯化铁,反应后溶液中含有铁离子,滴加KSCN溶液后溶液变为红色,溶液颜色变化明显,故D错误;
故选A.
点评 本题考查了铁离子、亚铁离子的检验方法,题目难度不大,明确铁及其化合物性质为解答关键,注意熟练掌握铁离子和亚铁离子的检验方法,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
9.下列有机物的结构、性质有关叙述正确的是( )
| A. | 分子式为C5H10O2,一定能与金属钠反应放出气体 | |
| B. | 甲苯分子中所有原子可能共面 | |
| C. | 生物柴油在NaOH溶液水解可得一种羧酸盐 | |
| D. | 乙醇、甲苯、葡萄糖能使酸性高锰酸钾溶液褪色 |
13.在一定温度下的密闭容器中,发生反应:A(s)+2B(g)═2C(g)+D(g),下列说法正确的是( )
| A. | 保持体积不变充入He气,体系压强增大,平衡逆向移动 | |
| B. | 保持压强不变充入He气,因为体系压强不变,所以平衡不移动 | |
| C. | 其它条件不变,向体系中加入A,A的转化率减小,B的转化率增大 | |
| D. | 其它条件不变,改变体积使压强改变,逆方向的速率改变的程度大于正方向 |
14.下列各组物质性质的比较中,错误的是( )
| A. | 还原性:HF<HCl<H2S | B. | 金属性:Na>Mg>Be | ||
| C. | 非金属性:F>Cl>S | D. | 离子半径:Al3+>Mg2+>F- |
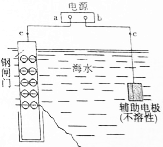 金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.
金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.