题目内容
将Fe、FeO、Fe3O4混合物均分成两等份,在相同条件下,一份用足量H2还原,参加反应H2的体积为V1,另一份用足量稀HNO3处理得NO气体体积为V2,若V1:V2=3:1,则原混合物中各成分的物质的量之比可能为( )
| A、2:3:2 |
| B、3:2:2 |
| C、1:2:3 |
| D、3:2:1 |
考点:有关混合物反应的计算
专题:计算题
分析:混合物和氢气反应生成Fe与水,水的物质的量等于混合物中O原子物质的量,混合物与足量浓硝酸反应生成NO,设各组分中FeO、Fe2O3、Fe3O4的物质的量分别为:x、y、z,根据O原子守恒与电子转移守恒列关系式判断.
解答:
解:将Fe、FeO、Fe3O4混合物均分成两等份,在相同条件下,一份用足量氢气还原,参加反应的H2体积为V1;另一份用足量稀HNO3处理后,生成NO的体积为V2若V1:V2=3:1;设各组分中铁、氧化亚铁、四氧化三铁物质的量分别为:x、y、z;
铁和氢气不反应,依据电子守恒得到,FeO~H2,Fe3O4~4H2,y+4z=V1;
另一份用足量稀HNO3处理后,铁、氧化亚铁、四氧化三铁中的亚铁被氧化为铁离子,生成NO的体积为V2;
Fe~NO
x x
3FeO~NO
y
y
3Fe3O4~NO
z
z
(y+4z):(x+
y+
z)=3:1,
得到x=z,
故选A.
铁和氢气不反应,依据电子守恒得到,FeO~H2,Fe3O4~4H2,y+4z=V1;
另一份用足量稀HNO3处理后,铁、氧化亚铁、四氧化三铁中的亚铁被氧化为铁离子,生成NO的体积为V2;
Fe~NO
x x
3FeO~NO
y
| 1 |
| 3 |
3Fe3O4~NO
z
| 1 |
| 3 |
(y+4z):(x+
| 1 |
| 3 |
| 1 |
| 3 |
得到x=z,
故选A.
点评:本题考查了铁及其化合物性质的分析计算应用,为高频考点,侧重于学生分析能力和计算能力的考查,掌握物质性质和四氧化三铁组成,氧化还原反应电子守恒是解题关键,题目难度中等.

练习册系列答案
相关题目
向50mL 0.018mol/LAgNO3溶液中加入50mL 0.02mol?L-1盐酸.已知AgCl(s)的溶度积常数Ksp=1×10-10,混合后溶液的体积变化忽略不计.下列说法不正确的是( )
| A、混合后,溶液中肯定有沉淀生成 |
| B、沉淀生成后溶液中Ag+的浓度为1×10-5 mol?L-1 |
| C、沉淀生成后溶液的pH=2 |
| D、混合后,升高温度,溶液中Ag+的浓度增大 |
正确的实验操作是实验成功的基本保证.下列实验操作正确的是( )
A、 检查装置气密性 |
B、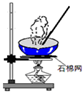 蒸发 |
C、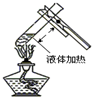 加热液体 |
D、 量取液体体积 |
只用一种试剂鉴别硫酸钠、硫酸镁、硫酸铝、硫酸铵四种溶液,这种试剂是( )
| A、氨水 | B、硝酸银溶液 |
| C、氢氧化钠 | D、盐酸 |
 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、Cl2和苛性钾溶液在不同温度下可能发生不同反应 |
| B、反应中转移电子数为是0.21 NA |
| C、原苛性钾溶液中KOH的物质的量无法确定 |
| D、生成物中Cl-的物质的量为 0.21 mol |
Al2O3
3
Al(OH)3,在以Al2O3为原料制备Al(OH)3时,X适宜用的试剂是( )
| HCl |
| X |
| A、NH3 |
| B、CO2 |
| C、NaOH |
| D、HCl |
下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A、10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合:C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
| B、10mL0.1mol/LNH1Cl与5mL0.2mol/LNaOH两溶液混合:C(Na+)=C(Cl-)>C(OH-)>C(H+) |
| C、10mL0.1mol/L醋酸与5mL0.2mol/L NaOH混合:C(Na+)=C(CH3COO-)>C(OH-)>C(H+) |
| D、10mL0.5mol/LCH3COONa溶液与6mL0.1mol/L盐酸混合:C(Cl-)>C(Na+)>C(OH-)>C(H+) |


 和
和 ,鉴别 I和J的试剂是
,鉴别 I和J的试剂是 制得,写出K在浓硫酸作用下生成的聚合物的结构简式:
制得,写出K在浓硫酸作用下生成的聚合物的结构简式: