题目内容
下列化学过程及其表述正确的是( )
| A、向NaHSO4溶液中滴入Ba(OH)2溶液至中性H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| B、由水电离的c(H+)为10-3mol?L-1的溶液中,Na+、NO3-、SO32-、Cl-定能大量共存 |
| C、酸碱中和滴定时,盛装标准液的滴定管滴定前无气泡,终点读数时有气泡,导致计算结果偏低 |
| D、可以用浓盐酸酸化的KMnO4溶液与H2O2混合,以证明H2O2具有还原性2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
考点:离子方程式的书写,离子共存问题,中和滴定
专题:离子反应专题
分析:A.至中性,反应生成硫酸钡、硫酸钠和水,生成硫酸钡和水的物质的量比为1:2;
B.由水电离的c(H+)为10-3mol?L-1的溶液,溶液显酸性,离子之间发生氧化还原反应;
C.盛装标准液的滴定管滴定前无气泡,终点读数时有气泡,则消耗的标准液V小,由C测=
分析;
D.浓盐酸酸化的KMnO4溶液,可与HCl发生氧化还原反应.
B.由水电离的c(H+)为10-3mol?L-1的溶液,溶液显酸性,离子之间发生氧化还原反应;
C.盛装标准液的滴定管滴定前无气泡,终点读数时有气泡,则消耗的标准液V小,由C测=
| c标V标 |
| V测 |
D.浓盐酸酸化的KMnO4溶液,可与HCl发生氧化还原反应.
解答:
解:A.向NaHSO4溶液中滴入Ba(OH)2溶液至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故A错误;
B.由水电离的c(H+)为10-3mol?L-1的溶液,溶液显酸性,H+、NO3-、SO32-发生氧化还原反应,不能大量共存,故B错误;
C.盛装标准液的滴定管滴定前无气泡,终点读数时有气泡,则消耗的标准液V小,由C测=
可知,计算结果偏低,故C正确;
D.用浓盐酸酸化的KMnO4溶液与H2O2混合,KMnO4溶液可与HCl发生氧化还原反应,则不能证明H2O2具有还原性,故D错误;
故选C.
B.由水电离的c(H+)为10-3mol?L-1的溶液,溶液显酸性,H+、NO3-、SO32-发生氧化还原反应,不能大量共存,故B错误;
C.盛装标准液的滴定管滴定前无气泡,终点读数时有气泡,则消耗的标准液V小,由C测=
| c标V标 |
| V测 |
D.用浓盐酸酸化的KMnO4溶液与H2O2混合,KMnO4溶液可与HCl发生氧化还原反应,则不能证明H2O2具有还原性,故D错误;
故选C.
点评:本题考查较综合,涉及离子反应书写的正误判断、离子共存、中和滴定及氧化还原反应等,为高频考点,把握物质的性质及反应原理为解答的关键,侧重高频考点的考查,题目难度中等.

练习册系列答案
相关题目
下列排列顺序不正确的是( )
| A、酸性:H3AsO4>H2SO4>H3PO4 |
| B、微粒的半径:Cl->Na+>Mg2+>Al3+ |
| C、热稳定性:HF>HCl>HBr>HI |
| D、熔点:SiO2>NaCl>I2 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、在标况下,11.2L NO与11.2L O2混合后所含分子数为0.75NA |
| B、常温常压下,16g O3所含的电子数为8NA |
| C、0.1mol Na2O2晶体中含有0.4NA个离子 |
| D、铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
用如图装置进行相应实验,不能达到实验目的是( )


| A、图1所示装置可制备氢氧化亚铁 |
| B、图2所示装置可电解食盐水制氯气和氢气 |
| C、图3所示装置可验证氨气极易溶于水 |
| D、图4所示装置与操作可除去苯中的苯酚 |
分类是化学研究的重要方法之一,下列有关说法中,正确的是( )
| A、SO2、NO2和CO2都属于酸性氧化物 |
| B、甲烷和和一氯甲烷都属于烷烃 |
| C、HC1O是弱电解质,NaClO却属于强电解质 |
| D、在水溶液中能电离出H+的化合物都属于酸 |
分子式为C9H11Cl的有机物,属于芳香族化合物且苯环上具有两个取代基的化合物共有(不考虑立体异构)( )
| A、9种 | B、12种 |
| C、15种 | D、18种 |
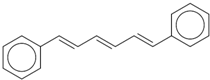 美国马丁?卡普拉等三位科学家因“在开发多尺度复杂化学系统模型”方面所做的贡献,获得了2013年诺贝尔化学奖.他们模拟出了1,6-二苯基-1,3,5-己三烯的分子模型,其结构简式如图所示.下列说法正确的是( )
美国马丁?卡普拉等三位科学家因“在开发多尺度复杂化学系统模型”方面所做的贡献,获得了2013年诺贝尔化学奖.他们模拟出了1,6-二苯基-1,3,5-己三烯的分子模型,其结构简式如图所示.下列说法正确的是( )| A、该有机物属于芳香烃,与苯互为同系物 |
| B、该有机物的分子式为C18H18 |
| C、1mol该有机物在常温下最多能与9mol Br2发生加成反应 |
| D、该有机物可以发生氧化反应、取代反应、加成反应 |
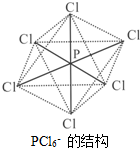 氮、磷属于同主族元素,广泛存在于生产生活的各种物质中.
氮、磷属于同主族元素,广泛存在于生产生活的各种物质中.