题目内容
20.将下列粒子的符号填入相应的空格内:O2、NH3、CO2、H2O、N2、(NH4)2SO4、SiCl4.(1)存在极性键的极性分子是NH3、H2O.
(2)存在非极性键的非极性分子是O2、N2.
(3)存在极性键的非极性分子是CO2、SiCl4.
(4)全部由非金属元素组成的离子化合物是(NH4)2SO4.
分析 一般活泼金属元素与活泼非金属元素形成离子键;同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键;结构对称,正负电荷的中心重合,则为非极性分子;结构不对称,正负电荷的中心不重合,则为极性分子;由离子键组成的化合物为离子化合物,据此分析.
解答 解:O2 只含有非极性键,属于非极性分子;
NH3只含极性键,为三角锥形结构,结构不对称,正负电荷的中心不重合,为极性分子;
CO2 只含极性键,为直线形分子,结构对称为非极性分子;
H2O 只含极性键,结构不对称,正负电荷的中心不重合,为极性分子;
N2为只含有非极性键的非极性分子;
(NH4)2SO4 含有共价键和离子键、配位键,属于离子化合物;
SiCl4只含极性键,为正四面体结构,结构对称为非极性分子;
(1)存在极性键的极性分子是NH3、H2O,故答案为:NH3、H2O;
(2)存在非极性键的非极性分子是O2、N2,故答案为:N2、O2;
(3)存在极性键的非极性分子是CO2、SiCl4,故答案为:CO2、SiCl4;
(4)全部由非金属元素组成的离子化合物是 (NH4)2SO4,故答案为:(NH4)2SO4.
点评 本题考查了键的极性和分子的极性、离子化合物的判断,题目综合性较强,侧重于基础知识的考查,题目难度不大,注意掌握分子极性的判断方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列电离方程式正确的是( )
| A. | Na2CO3→Na++CO32- | B. | H2S→2H++S2- | ||
| C. | H2CO3→H++HCO3- | D. | NaHSO4→Na++H++SO42- |
15.以下能级符号不正确的是( )
| A. | 6s | B. | 2d | C. | 3p | D. | 7f |
5.下列实验装置正确且能达到实验目的是( )
| A. | 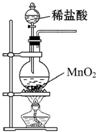 制取少量Cl2 | |
| B. | 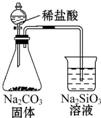 证明非金属性Cl>C>Si | |
| C. | 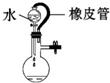 水不能持续流下,说明装置气密性良好 | |
| D. | 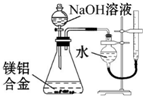 测定镁铝合金中铝的质量分数 |
12.某有机物的结构简式如图所示,下列有关该有机物的说法中正确的是( )
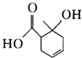

| A. | 能和碳酸钠溶液反应的官能团有2种 | |
| B. | 1mol该有机物最多能与2molH2发生加成 | |
| C. | 与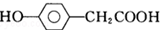 互为同分异构体 互为同分异构体 | |
| D. | 既可以发生取代反应又可以发生氧化反应 |
9.下列物质的分离提纯所用的方法不正确的是( )
| A. | 酒精和水:分液 | |
| B. | 淀粉溶液(胶体)中混有氯化钠:用半透膜进行渗析 | |
| C. | 汽油和柴油:分馏 | |
| D. | 三氯甲烷和水:分液 |
10.反应4NH3+5O2=4NO+6H2O 在5L的密闭容器中进行,30s后,NO的物质的量增加了0.3mol,则此反应的平均速率可表示为( )
| A. | v(O2)=0.0025 mol/(L•s) | B. | v(NO)=0.008 mol/(L•s) | ||
| C. | v(H2O)=0.003 mol/(L•s) | D. | v(NH3)=0.002 mol/(L•s) |
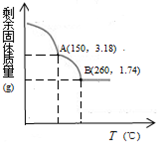 某铜(Ⅱ)盐晶体组成可以表示为Ka[Cub(C2O4)c]•dH2O,其组成可通过下列实验测定:
某铜(Ⅱ)盐晶体组成可以表示为Ka[Cub(C2O4)c]•dH2O,其组成可通过下列实验测定: