题目内容
13.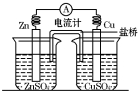 将锌片、铜片、盐桥、导线、电流计和ZnSO4溶液、CuSO4溶液连接成如图装置,下列各叙述中正确的是( )
将锌片、铜片、盐桥、导线、电流计和ZnSO4溶液、CuSO4溶液连接成如图装置,下列各叙述中正确的是( )| A. | 构成原电池,锌片作正极 | |
| B. | 铜片附近Cu2+离子浓度减小 | |
| C. | 锌片上有铜析出,铜片上没有 | |
| D. | 导线中电流的方向是由锌片流向铜片 |
分析 将锌片、铜片、盐桥、导线、电流计和ZnSO4溶液、CuSO4溶液构成的原电池中,金属锌是负极,铜是正极,自发的氧化还原反应是金属锌和硫酸铜之间的反应,根据原电池的工作原理来回答.
解答 解:A.将锌片、铜片、盐桥、导线、电流计和ZnSO4溶液、CuSO4溶液构成的原电池中,金属锌是负极,故A错误;
B.铜片是正极,电解质中的阳离子铜离子移向正极,在该极上得电子,析出金属铜,所以Cu片附近Cu2+离子浓度减小,故B正确;
C.负极上是金属锌溶解,正极Cu上Cu2+得电子析出金属铜,故C错误;
D.电流从正极流出,即从铜片流向锌片,故D错误.
故选B.
点评 本题考查学生盐桥原电池的工作原理知识,注意正负极的判断以及电解质中阴阳离子的移动是解题的关键,题目难度不大.

练习册系列答案
相关题目
3.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 等质量的N2和CO所含分子数均为NA | |
| B. | 在标准状况下,22.4 L CH4与NH3的混合气体所含的电子数为10NA | |
| C. | 标准状况下,224 mL水含有的电子数为0.1 NA | |
| D. | 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
4.根据如图所示的信息,判断下列叙述不正确的是( )
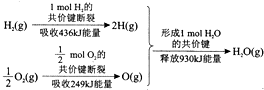

| A. | 1molH2(g)的共价键形成放出436kJ能量 | |
| B. | 氢气跟氧气反应生成水的同时吸收能量 | |
| C. | 1molH2(g)跟$\frac{1}{2}$molO2(g)反应生成1molH2O(g)释放能量245kJ | |
| D. | 1molH2(g)与$\frac{1}{2}$molO2(g)的总能量大于1molH2O(g)的能量 |
8.β-月桂烯的结构如图所示,该物质与Br2按物质的量之比为1:1加成时,所得产物有( )
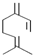

| A. | 2种 | B. | 3种 | C. | 4种 | D. | 6种 |


