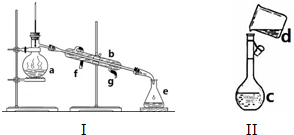
题目内容
下述实验不能达到预期实验目的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 将2.5g CuSO4?5H2O溶解在97.5g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 取少量待检固体溶于水中,滴加少量Ba(OH)2溶液,观察是否有白色沉淀生成 | 检验NaHCO3固体中是否含Na2CO3 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,分液和萃取,配制一定物质的量浓度的溶液
专题:实验评价题
分析:A.2.5gCuSO4?5H2O中CuSO4的质量为2.5g×
=1.6g;
B.根据沉淀的转化来分析;
C.Na2CO3能与Ba(OH)2溶液发生反应生成BaCO3沉淀,NaHCO3也能与Ba(OH)2溶液发生反应生成BaCO3沉淀;
D.上层液体从上口倒出.
| 160 |
| 250 |
B.根据沉淀的转化来分析;
C.Na2CO3能与Ba(OH)2溶液发生反应生成BaCO3沉淀,NaHCO3也能与Ba(OH)2溶液发生反应生成BaCO3沉淀;
D.上层液体从上口倒出.
解答:
解:A.2.5gCuSO4?5H2O中CuSO4的质量为2.5g×
=1.6g,溶液的质量为2.5g+97.5g=100g,则配制质量分数为1.6%的CuSO4溶液,故A正确;
B.因硫化银比氯化银更难溶,则向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液,会得到黑色沉淀,说明一种沉淀能转化为另一种更难溶的沉淀,故B正确;
C.Na2CO3能与Ba(OH)2溶液发生反应生成BaCO3沉淀,NaHCO3也能与Ba(OH)2溶液发生反应生成BaCO3沉淀,故不能用Ba(OH)2溶液检验NaHCO3固体中是否含Na2CO3,可以用BaCl2溶液检验,故C错误;
D.为防止试剂受污染,则分层后,上层液体从上口倒出,下层液体从下口流出,故D正确.
故选C.
| 160 |
| 250 |
B.因硫化银比氯化银更难溶,则向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液,会得到黑色沉淀,说明一种沉淀能转化为另一种更难溶的沉淀,故B正确;
C.Na2CO3能与Ba(OH)2溶液发生反应生成BaCO3沉淀,NaHCO3也能与Ba(OH)2溶液发生反应生成BaCO3沉淀,故不能用Ba(OH)2溶液检验NaHCO3固体中是否含Na2CO3,可以用BaCl2溶液检验,故C错误;
D.为防止试剂受污染,则分层后,上层液体从上口倒出,下层液体从下口流出,故D正确.
故选C.
点评:本题考查了在化学实验中基本操作,难度不大,溶液的配置、分液的操作都是在此类试题中易考查的方向,在进行物质的检验中注意物质的性质的区别和联系是本题的关键,属于易错试题.

练习册系列答案
相关题目
用10mL的0.1mol/L BaCl2溶液恰好可使相同体积的硫酸铝、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
| A、3:2:2 |
| B、1:3:3 |
| C、2:3:6 |
| D、3:1:1 |
甲萘醌(维生素K)有止血作用,它可通过2-甲基萘的氧化而制得,反应中常用乙酸作催化剂,该反应放热,可表示为: ,在某次合成反应中,用1.4g的2-甲基萘,才制得0.17g甲萘醌,已知该次合成反应的速率是快的,试判断导致其产率低的原因是( )
,在某次合成反应中,用1.4g的2-甲基萘,才制得0.17g甲萘醌,已知该次合成反应的速率是快的,试判断导致其产率低的原因是( )
 ,在某次合成反应中,用1.4g的2-甲基萘,才制得0.17g甲萘醌,已知该次合成反应的速率是快的,试判断导致其产率低的原因是( )
,在某次合成反应中,用1.4g的2-甲基萘,才制得0.17g甲萘醌,已知该次合成反应的速率是快的,试判断导致其产率低的原因是( )| A、使用了过量的氧化剂 |
| B、没有用乙酸,而是使用了其它催化剂 |
| C、把反应混合物加热 |
| D、所生成的甲萘醌是沉淀物 |
欲使CuSO4?5H2O、NH4Cl和SiO2的混合物分离开来,其必要的实验操作为( )
| A、加热 溶解 过滤 结晶 |
| B、溶解 过滤 蒸发 结晶 |
| C、加热 溶解 蒸发 过滤 |
| D、溶解 过滤 蒸馏 蒸发 |
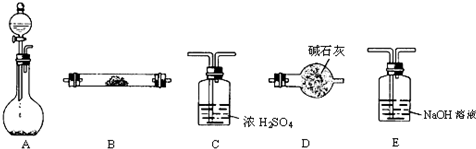
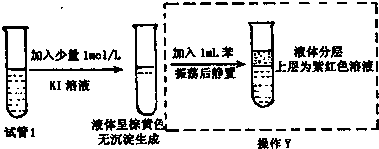
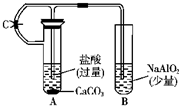 利用如图所示装置进行相关试验,验证铝的化合物的相关性质.请回答:
利用如图所示装置进行相关试验,验证铝的化合物的相关性质.请回答: