题目内容
下列各溶液中,Na+ 浓度最大的是( )
| A、5 L 1.2 mol?L-1的Na2SO4溶液 |
| B、2 L 0.8 mol?L-1的NaOH溶液 |
| C、1 L 1 mol?L-1的Na2CO3溶液 |
| D、4 L 0.5 mol?L-1的NaCl溶液 |
考点:物质的量浓度的相关计算
专题:
分析:根据溶液中溶质的物质的量浓度以及物质的化学式构成计算出Na+的物质的量浓度,然后再进行进行比较钠离子浓度大小大小,注意钠离子浓度与溶液的体积无关.
解答:
解:A.c(Na+)=2×c(Na2SO4)=2.4mol/L;
B.c(Na+)=c(NaOH)=0.8mol/L;
C.c(Na+)=2c(Na2CO3)=2mol/L;
D.c(Na+)=c(NaCl)=0.5mol/L;
则浓度最大的是A,
故选A.
B.c(Na+)=c(NaOH)=0.8mol/L;
C.c(Na+)=2c(Na2CO3)=2mol/L;
D.c(Na+)=c(NaCl)=0.5mol/L;
则浓度最大的是A,
故选A.
点评:本题考查物质的量浓度的大小比较,注意各物质的化学式构成,明确离子的物质的量浓度与溶液物质的量浓度的关系,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1体积pH=2的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( )
| A、8.0 | B、9.0 |
| C、10.0 | D、11.0 |
如图是10mL量筒的一部分,A与C之间相差1mL,如果刻度A为5,则量筒所盛液体的体积是( )mL.
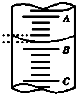

| A、5.8 | B、4.4 |
| C、4.2 | D、4.6 |
x、y为短周期元素,x原子K、L、M各电子层的电子数之比为1:4:1,它比y原子多3个电子,下列叙述正确的是( )
| A、x离子半径大于y离子半径 |
| B、x单质在空气中燃烧可生成两种化合物 |
| C、x位于第三周期ⅣA族 |
| D、y的最高正价小于x的最高正价 |
下列说法不正确的是( )
| A、CH3-CH=CH2和CH2=CH2的最简式相同 |
| B、CH≡CH和C6H6含碳量相同 |
| C、正戊烷、异戊烷、新戊烷的沸点依次降低 |
| D、乙二醇和丙三醇为同系物 |
120mL含有0.20mol碳酸钠的溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A、0.18mol/L |
| B、0.24mol/L |
| C、2.0mol/L |
| D、1.5mol/L |
下列说法中正确的是( )
| A、离子化合物中只有离子键,没有共价键 |
| B、全部由非金属构成的化合物中只有共价键 |
| C、电子数相同的两种微粒一定是同一种元素 |
| D、化学变化一定有化学键的变化 |