题目内容
有以下物质:①NaOH ②Na2O2 ③HClO ④MgCl2 ⑤K2SO4 ⑥Ne(用序号作答)
(1)只含有离子键的是 ;
(2)只含有共价键的是 ;
(3)没有化学键的是 ;
(4)既有离子键,又有非极性共价键的是 ;
(5)属于共价化合物的是 ;
(6)属于离子化合物且阴阳离子个数比为2:1的是 .
(1)只含有离子键的是
(2)只含有共价键的是
(3)没有化学键的是
(4)既有离子键,又有非极性共价键的是
(5)属于共价化合物的是
(6)属于离子化合物且阴阳离子个数比为2:1的是
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型,极性键和非极性键
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,只含共价键的化合物是共价化合物,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,铵盐都属于离子化合物,据此分析解答.
解答:
解:①NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,属于离子化合物;
②Na2O2中钠离子和过氧根离子之间存在离子键、O原子之间存在共价键,属于离子化合物;
③HClO中O原子和H原子、Cl原子之间只存在共价键,属于共价化合物;
④MgCl2中镁离子和氯离子之间只存在离子键,属于离子化合物;
⑤K2SO4中钾离子和硫酸根离子之间存在离子键,S原子和O原子之间存在共价键,属于离子化合物;
⑥Ne是单原子分子,不存在化学键;
(1)只含有离子键的是④,故答案为:④;
(2)只含有共价键的是③,故答案为:③;
(3)没有化学键的是 ⑥,故答案为:⑥;
(4)既有离子键,又有非极性共价键的是②,故答案为:②;
(5)属于共价化合物的是③,故答案为:③;
(6)属于离子化合物且阴阳离子个数比为2:1的是④,故答案为:④.
②Na2O2中钠离子和过氧根离子之间存在离子键、O原子之间存在共价键,属于离子化合物;
③HClO中O原子和H原子、Cl原子之间只存在共价键,属于共价化合物;
④MgCl2中镁离子和氯离子之间只存在离子键,属于离子化合物;
⑤K2SO4中钾离子和硫酸根离子之间存在离子键,S原子和O原子之间存在共价键,属于离子化合物;
⑥Ne是单原子分子,不存在化学键;
(1)只含有离子键的是④,故答案为:④;
(2)只含有共价键的是③,故答案为:③;
(3)没有化学键的是 ⑥,故答案为:⑥;
(4)既有离子键,又有非极性共价键的是②,故答案为:②;
(5)属于共价化合物的是③,故答案为:③;
(6)属于离子化合物且阴阳离子个数比为2:1的是④,故答案为:④.
点评:本题考查化学键的判断,侧重考查化学基本概念,注意离子键和共价键的区别,注意:并不是所有的物质都含有化学键,稀有气体不含化学键,为易错点.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
 如图,Ⅰ是恒压密闭容器,Ⅱ是恒容刚性密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?aZ(g).则Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容刚性密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?aZ(g).则Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )| A、若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ<Ⅱ |
| B、若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| C、若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间相同 |
| D、平衡时Ⅰ容器的体积小于V L |
下列物质中所含分子物质的量最多的是( )
| A、44 g CO2 |
| B、1.5 mol H2 |
| C、64 g SO2 |
| D、3.01×1023个硫酸分子 |
氢键既可以存在于分子之间,也可以存在于分子内部的原子团之间,如邻羟基苯甲醛分子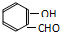 ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子(
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( 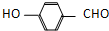 )之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )
)之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )
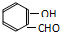 ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子(
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子(  )之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )
)之间存在氢键(分子间氢键).则两者的熔点、沸点的相对大小关系是( )| A、前者>后者 | B、前者<后者 |
| C、前者=后者 | D、无法估计 |
我国歼-10战斗机利用现代科技将
Po涂于飞机表面,可以吸收和屏蔽雷达和红外线辐射,起到一定的隐身作用.该Po(钋)原子核外电子数是( )
209 84 |
| A、209 | B、125 |
| C、84 | D、42 |
下列有关阿伏加德罗常数(NA)的说法不正确的是( )
| A、0.012 kg12C所含有的碳原子数为NA个 |
| B、NA的近似值为6.02×1023 |
| C、1 mol H2O含有的H2O分子数目为NA个 |
| D、NA个Cl2的质量为35.5 g |
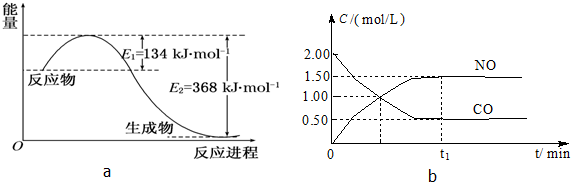
图1表示mA(g)+nB(g)?pC(g)+qD(g)△H=-Q,在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;图2表示在一定条件下达到平衡后t时刻(温度不变)改变影响平衡的另一个条件重新建立新平衡的反应过程,判断该反应是 ( )
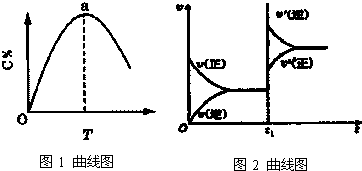

| A、m+n>p+q Q>0 |
| B、m+n>p+q Q<0 |
| C、m+n<p+q Q>0 |
| D、m+n<p+q Q<0 |