题目内容
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、25℃时,56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
| C、常温下,1.20 g NaHSO4固体中含有的阴阳离子总数为0.3 NA |
| D、78 g Na2O2和Na2S的混合物中含有的阴离子数为NA |
考点:阿伏加德罗常数
专题:
分析:A.亚铁离子和碘离子都能够被氯气氧化,1mol碘化亚铁完全反应消耗1.5mol氯气;
B、常温下,铁在浓硫酸中会钝化;
C、NaHSO4固体中含1mol钠离子和1molHSO4-;
D、Na2O2和Na2S均由2个阳离子和1个阴离子构成来分析.
B、常温下,铁在浓硫酸中会钝化;
C、NaHSO4固体中含1mol钠离子和1molHSO4-;
D、Na2O2和Na2S均由2个阳离子和1个阴离子构成来分析.
解答:
解:A.1molFeI2中含有1mol亚铁离子、2mol碘离子,完全反应需要消耗1.5mol氯气,转移了3mol电子,转移的电子数为3NA,故A错误;
B、常温下,铁在浓硫酸中会钝化,故B错误;
C、1.20 g NaHSO4固体的物质的量为0.01mol,而NaHSO4固体中含1mol钠离子和1molHSO4-,故0.01molNaHSO4中含有的离子为0.02mol,故C错误;
D、Na2O2和Na2S的摩尔质量均为78g/mol,故78g的Na2O2和Na2S混合物的物质的量为1mol,而Na2O2和Na2S均由2个阳离子和1个阴离子构成,故1molNa2O2和Na2S混合物中含1mol阴离子,个数为NA个,故D正确.
故选D.
B、常温下,铁在浓硫酸中会钝化,故B错误;
C、1.20 g NaHSO4固体的物质的量为0.01mol,而NaHSO4固体中含1mol钠离子和1molHSO4-,故0.01molNaHSO4中含有的离子为0.02mol,故C错误;
D、Na2O2和Na2S的摩尔质量均为78g/mol,故78g的Na2O2和Na2S混合物的物质的量为1mol,而Na2O2和Na2S均由2个阳离子和1个阴离子构成,故1molNa2O2和Na2S混合物中含1mol阴离子,个数为NA个,故D正确.
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
在下列五种物质的组合中,既能跟氢氧化钠溶液反应,又能跟盐酸反应的化合物是( )
①Al ②Al(OH)3 ③Al2O3 ④Na2CO3 ⑤NaHCO3.
①Al ②Al(OH)3 ③Al2O3 ④Na2CO3 ⑤NaHCO3.
| A、①②③⑤ | B、①③④⑤ |
| C、②③⑤ | D、②④⑤ |
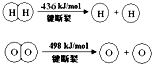 已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,下列说法不正确的是( )
已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,下列说法不正确的是( )| A、该反应原理可用于设计氢氧燃料电池 | ||
| B、破坏1 mol H-O 键需要的能量是463.4 kJ | ||
C、H2O(g)=H2(g)+
| ||
| D、H2(g) 中的H-H 键比 H2O(g) 中的H-O 键牢固 |
 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是( )| A、气态氢化物稳定性:W>Y |
| B、Z与Q形成的化合物水溶液不一定显酸性 |
| C、Y的单质比W的单质沸点高 |
| D、原子半径从大到小排列是:Z>X>Y>W>Q |
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、4℃时,5.4mL水中所含的水分子数是0.3NA(4℃时,水的密度为1.0g/ml) |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为 NA |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3 NA |
下列说法正确的是( )
| A、H2的摩尔质量是2mol |
| B、CO2的摩尔质量是44g/mol |
| C、1mol的氧 |
| D、3molO2的摩尔质量为96g/mol |
已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G-→Q+NaCl
②Q+H2O
X+H2
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
①G-→Q+NaCl
②Q+H2O
| ||
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
| A、G、Y、Q、Z、X |
| B、X、Z、Q、G、Y |
| C、X、Z、Q、Y、G |
| D、G、Q、Y、Z、X |
下列指定反应的离子方程式正确的是( )
| A、铜溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B、氯气和水的反应:Cl2+H2O=2H++Cl-+ClO- |
| C、用氨水溶解氯化银沉淀:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O |
| D、将过量二氧化硫通入氨水中:SO2+NH3?H2O=HSO3-+NH4+ |