题目内容
17.已知90℃时水的离子积常数为KW=1×10-12,在90℃时,若将体积为Va、pH=a的某一元强酸溶液A与体积为Vb、pH=b的某一元强碱溶液B混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白:(1)a值可否等于3?否(填“可”或“否”),其理由是a=3,此时b=6,B不是一元强碱.
(2)a值可否等于4?否(填“可”或“否”),其理由是两溶液混合后溶液恰好为中性,则:Va•c(H+)=Vb•c(OH-),$\frac{Va}{Vb}$=$\frac{c(O{H}^{-})}{c({H}^{+})}$=$\frac{\frac{1{0}^{-12}}{1{0}^{-b}}}{1{0}^{-a}}$=10a+b-12<1,若a=4,则b=8,所以a+b-12=0,此时和Va<Vb即(a+b-12)<0矛盾.
(3)a值的取值范围是3.5<a<4.
分析 体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,则:Va•10-a=Vb•10b-12,结合Va<Vb和a=0.5b进行计算和判断.
解答 解:两溶液混合后溶液恰好为中性,则:Va•c(H+)=Vb•c(OH-),$\frac{Va}{Vb}$=$\frac{c(O{H}^{-})}{c({H}^{+})}$=$\frac{\frac{1{0}^{-12}}{1{0}^{-b}}}{1{0}^{-a}}$=10a+b-12<1,所以(a+b-12)<0,而a=0.5b,
即3a<12,a<4,又pH=b=2a>7,a>3.5,所以3.5<a<4,
(1)a值不能等于3,a=3,此时b=6,因pH=b的是一元强碱,b应该是大于7的,故答案为:否;a=3,此时b=6,B不是一元强碱;
(2)a值不能等于4,因为两溶液混合后溶液恰好为中性,则:Va•c(H+)=Vb•c(OH-),$\frac{Va}{Vb}$=$\frac{c(O{H}^{-})}{c({H}^{+})}$=$\frac{\frac{1{0}^{-12}}{1{0}^{-b}}}{1{0}^{-a}}$=10a+b-12<1,若a=4,则b=8,所以a+b-12=0,此时和Va<Vb即(a+b-12)<0矛盾,
故答案为:否;两溶液混合后溶液恰好为中性,则:Va•c(H+)=Vb•c(OH-),$\frac{Va}{Vb}$=$\frac{c(O{H}^{-})}{c({H}^{+})}$=$\frac{\frac{1{0}^{-12}}{1{0}^{-b}}}{1{0}^{-a}}$=10a+b-12<1,若a=4,则b=8,所以a+b-12=0,此时和Va<Vb即(a+b-12)<0矛盾;
(3)a值的取值范围是3.5<a<4,故答案为:3.5<a<4.
点评 本题考查酸碱混合的定性判断和溶液pH的有关计算,题目难度中等,注意酸碱混合时酸碱物质的量的关系以及溶液pH与c(H+)、(OH-)的关系.

| A. | 金属原子的最外层电子数一定不大于4 | |
| B. | 黑色金属只包括铁、铬、锰 | |
| C. | 金属氧化物一定是碱性氧化物 | |
| D. | 金属元素既有正化合价又有负价 |
| A. | 元素B的化合物可以用来做焰火材料 | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 元素B、D的最高价氧化物对应的水化物之间可能发生反应 |
| A. | 化合物 | B. | 氧化物 | C. | 无机物 | D. | 钾盐 |
| A. | Fe3+、NH${\;}_{4}^{+}$、Br-、I- | B. | Fe2+、H+、NO3-、Cl- | ||
| C. | Fe3+、H+、SO42-、Br- | D. | Fe3+、Ca2+、NO3-、SO42-、 |
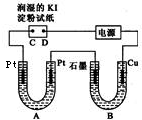 电解装置如图所示,图中B装置盛有1L2mol•L-1的Na2SO4溶液,A装置盛有1L2mol•L-1的AgNO3溶液,通电后,湿润的淀粉KI试纸的C端变蓝色,电解一段时间后,试回答:
电解装置如图所示,图中B装置盛有1L2mol•L-1的Na2SO4溶液,A装置盛有1L2mol•L-1的AgNO3溶液,通电后,湿润的淀粉KI试纸的C端变蓝色,电解一段时间后,试回答: