题目内容
(14分)金属铜具有良好的导电性和导热性,在电气和电子工业中应用广泛。请回答下列问题:
(1)资料显示:加热条件下氨气能够还原CuO得到金属铜。某同学用装置I和Ⅱ制取纯净干燥的氨气,装置I中应选用试剂______(供选用的试剂有:NH4Cl固体、NH4HCO3固体),试剂a最好选用__________,其作用是_________________________________________;装置III吸收尾气,如何检验所得溶液中数目最多的阳离子(只回答试剂名称和实验现象)_____________________。

(2)电解硫酸铜溶液也可得到金属铜。
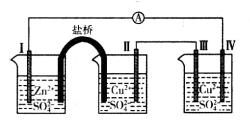
①以黄铜矿(主要成份为CuFeS2)为原料采用电解法可制取硫酸铜溶液。实验室用如图所示装置模拟其过程,阳极区稀硫酸的作用是溶解矿粉得到Cu2+、Fe2+、H2S,硫酸铁的作用是氧化吸收H2S,防止逸出造成污染。电解过程中,阳极区Fe3+的浓度基本保持不变,原因是(用电极反应式回答)______________,阴极上先有固体析出,然后又溶解,阴极区通入O2的作用是(用离子方程式回答)__________________。

②用惰性电极电解一定浓度CuSO4溶液制取金属铜,一段时间后停止通电,此时加入9.8gCu(OH)2恰好能使电解质溶液恢复至初始状态,则该过程中阳极产生气体的体积为____________L(标准状况)。
(1)NH4HCO3(固体);碱石灰;除去H2O和CO2;NaOH溶液、湿润的红色石蕊试纸、变蓝
(2)Fe2+-e-=Fe3+;2Cu+O2+4H+=2Cu2++2H2O;2.24
【解析】
试题分析:(1)装置I是固体加热制备氨气,由于氯化铵分解生成的氨气冷却后又会重新结合为氯化铵,而碳酸氢铵分解生成氨气、CO2和水,利用碱石灰除去CO2和水即可制备氨气,因此装置I中应选用试剂是碳酸氢铵;氨气溶于水生成一水合氨,一水合氨电离出铵根离子,因此溶液中阳离子最多的是铵根离子。铵根离子能与碱反应生成氨气,氨气是碱性气体,能使湿润的红色试纸变为蓝色,据此可以检验铵根离子;
(2)①铁离子能氧化H2S生成亚铁离子,但在阳极区溶液中的亚铁离子失去电子转化为铁离子,从而导致溶液中铁离子浓度基本保持不变,电极反应式为Fe2+-e-=Fe3+;氧气具有强氧化性,在稀硫酸溶液中能与氧化析出的铜转化为硫酸铜,离子方程式为2Cu+O2+4H+=2Cu2++2H2O;
②用惰性电极电解一定浓度CuSO4溶液制取金属铜,阳极始终是溶液中的氢氧根离子放电,而阴极先是溶液中的铜离子放电,然后是溶液中的氢离子放电。所以一段时间后停止通电,此时若加入9.8gCu(OH)2恰好能使电解质溶液恢复至初始状态,这说明阴极上氢离子也放电。9.8g氢氧化铜的物质的量是0.1mol,则根据氧原子守恒可知,阴极生成的氧气是0.1mol,在标准状况下的体积是2.24L。
考点:考查氨气制备、铵根离子检验以及电化学原理的应用


 3C+4D中,下列表示该反应速率最快的是
3C+4D中,下列表示该反应速率最快的是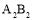
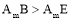
 →电极I
→电极I
 )>c(Fe2+)>c(H+)
)>c(Fe2+)>c(H+) )+c(
)+c(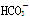 )+c(OH-)
)+c(OH-)