题目内容
14.下列各组离子在溶液中能大量共存的是( )| A. | Ca2+、HCO3-、Cl-、K+ | B. | Al3+、AlO2-、H+、Na+ | ||
| C. | Fe2+、NH4+、SO42-、S2- | D. | Fe3+、SCN-、Na+、CO32- |
分析 A.四种离子之间不发生反应,能够共存;
B.铝离子、氢离子都与偏铝酸根离子反应;
C.亚铁离子与硫离子发生反应;
D.铁离子与硫氰根离子、碳酸根离子反应.
解答 解:A.Ca2+、HCO3-、Cl-、K+之间不反应,在溶液中可以大量共存,故A正确;
B.Al3+、H+都与AlO2-发生反应,在溶液中不能大量共存,故B错误;
C.Fe2+、S2-之间反应,在溶液中不能大量共存,故C错误;
D.Fe3+与SCN-、CO32-发生反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
5.某无色溶液中一定能大量共存的离子组是( )
| A. | Cu2+、Na+、NO3-、SO42- | B. | Ba2+、NH4+、Cl-、SO42- | ||
| C. | Na+、K+、ClO-、SO42- | D. | H+、Na+、I-、NO3- |
2.设阿伏加德常数为NA,则下列说法正确的是( )
| A. | 1 L 0.1 mol/L MgCl2溶液中含Cl-数为0.1NA | |
| B. | 1mol Na完全转化为Na2O2时,失去的电子数目为2NA | |
| C. | 含有NA个氢原子的氢气的体积约为11.2L | |
| D. | 1.8g NH4+中所含电子数为NA |
19.将蔗糖用少量水润湿后,一边搅拌一边慢慢加入浓硫酸,可以看到这样颜色逐渐变黑,体积不断膨胀,最终变成疏松多孔的海绵状固体,且伴有刺激性气味.上述过程中体现出浓硫酸( )
| A. | 只有强氧化性 | B. | 只有脱水性 | ||
| C. | 既有吸水性又有脱水性 | D. | 有吸水性、脱水性、氧化性 |
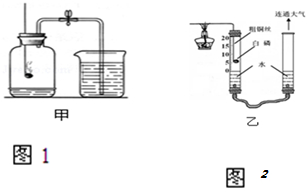
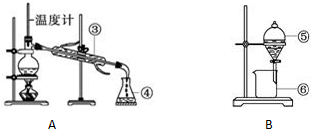
3.用下列实验装置完成对应的实验(部分仪器已省),能达到实验目的是( )
| A. | 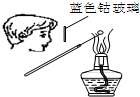 检验Na2CO3中的Na+ | B. | 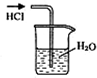 吸收HCl | ||
| C. | 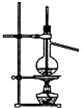 石油的蒸馏 | D. | 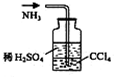 吸收NH3 |
8.反应:①PCl5(g)═PCl3(g)+Cl2(g) ②2HI(g)═H2(g)+I2(g)③2NO2(g)═N2O4(g)在一定条件下,达到化学平衡时,反应物的转化率均是a%,若保持各反应的温度和容器的体积都不改变,分别再加入一定量的各自的反应物,则转化率( )
| A. | ①减小,②不变,③减小 | B. | ①增大,②不变,③减小 | ||
| C. | ①增大,②不变,③增大 | D. | ①减小,②不变,③增大 |