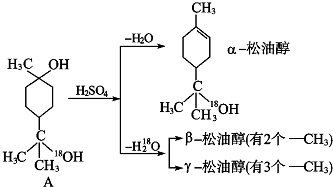
题目内容
 现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子X、Cl-、OH-、NO3-、CO32-中的一种.
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子X、Cl-、OH-、NO3-、CO32-中的一种.(1)某同学通过比较分析,认为无须检验就可判断其中必有的两种物质是
(2)物质C中含有离子X.为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体.则X为
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式
(4)若用惰性电极电解C和D的混合溶液,溶质的物质的量均为0.1mol,请在坐标系中画出通电后阴极上析出固体的质量m与通过电子的物质的量n的关系(标明纵坐标数值).
(5)25℃时,硫酸钡的Ksp=1.0×10-10,碳酸钡的Ksp=2.5×10-9,若向20mL硫酸钡的饱和溶液中逐滴加入8.0×10-4mol/L的碳酸钠溶液20mL,能否产生沉淀
考点:常见阳离子的检验,难溶电解质的溶解平衡及沉淀转化的本质,常见阴离子的检验
专题:物质检验鉴别题
分析:CO32-与Fe3+、Cu2+、Ba2+、Al3+不能大量共存,OH-与Fe3+、Cu2+、Al3+不能大量共存;则必有的两种物质记为A、B,A、B分别为K2CO3、Ba(OH)2,C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,蓝色沉淀为氢氧化铜,白色沉淀为硫酸钡,则A应为Ba(OH)2,C中含SO42-,则C为CuSO4,D为Al(NO3)3,E为FeCl3,据此分析解答即可.
解答:
解:CO32-与Cu2+、Ba2+、Fe3+、Al3+不能大量共存,OH-与Fe3+、Al3+、Cu2+不能大量共存,则必有的两种物质记为A、B,A、B分别为K2CO3、Ba(OH)2,C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,蓝色沉淀为氢氧化铜,白色沉淀为硫酸钡,则A应为Ba(OH)2,C中含SO42-,则C为CuSO4,D为Al(NO3)3,E为FeCl3.
(1)由上述分析可知,必有的两种物质为K2CO3、Ba(OH)2,故答案为:K2CO3;Ba(OH)2;
(2)由上述分析可知,C为CuSO4,C中X为SO42-,故答案为:B;
(3)根据以上推断可知D中含有NO3-,已知将19.2gCu投入装有足量D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,
发生的反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
则n(Cu)=mM=
=0.3mol,
有方程可知
=
,
所以n(H+)=0.8mol,
所以n(H2SO4)=12n(H+)=0.4mol,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.4mol;
(4)若用惰性电极电解CuSO4和Al(NO3)的混合溶液,溶质的物质的量均为0.1mol,故答案为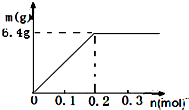 ;
;
首先,阴极发生反应:Cu2++2e-=Cu,则n(电子)=0.1×2=0.2mol,即m=0.1mol×64g/mol=6.4g;
(5)已知25℃时硫酸钡的Ksp=1.0×10-10,若向20mL硫酸钡的饱和溶液中逐滴加入8.0×10-4mol/L的Na2CO3溶液20mL,混合后溶液中c(Ba2+)≈
×
mol/L=5.0×10-6mol/L,则溶液中c(CO32-)=
×8.0×10-4mol/L=4.0×10-4mol/L,而5.0×10-6×4.0×10-4=2.0×10-9<2.5×10-9,故没有沉淀产生,
故答案为:否.
(1)由上述分析可知,必有的两种物质为K2CO3、Ba(OH)2,故答案为:K2CO3;Ba(OH)2;
(2)由上述分析可知,C为CuSO4,C中X为SO42-,故答案为:B;
(3)根据以上推断可知D中含有NO3-,已知将19.2gCu投入装有足量D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,
发生的反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
则n(Cu)=mM=
| 19.2g |
| 64g/mol |
有方程可知
| 3 |
| 8 |
| 0.3mol |
| n(H+) |
所以n(H+)=0.8mol,
所以n(H2SO4)=12n(H+)=0.4mol,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.4mol;
(4)若用惰性电极电解CuSO4和Al(NO3)的混合溶液,溶质的物质的量均为0.1mol,故答案为
 ;
;首先,阴极发生反应:Cu2++2e-=Cu,则n(电子)=0.1×2=0.2mol,即m=0.1mol×64g/mol=6.4g;
(5)已知25℃时硫酸钡的Ksp=1.0×10-10,若向20mL硫酸钡的饱和溶液中逐滴加入8.0×10-4mol/L的Na2CO3溶液20mL,混合后溶液中c(Ba2+)≈
| 1 |
| 2 |
| 1.0×10-10 |
| 1 |
| 2 |
故答案为:否.
点评:本题综合性较强,涉及无机物推断、离子检验、盐类水解、离子浓度比较、电解原理等,需要学生熟练掌握基础知识,有利于考查学生的推理能力,难度中等.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的主要反应之一.一定温度下,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示下列判断中,正确的是( )
| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | |
| A、乙中SO2的平衡转化率大于80% |
| B、该温度下,乙达平衡时间小于甲 |
| C、平衡时,丙中c(SO3)是甲中的2倍 |
| D、平衡时,甲中O2的转化率大于乙中O2的转化率 |

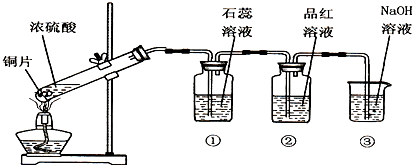
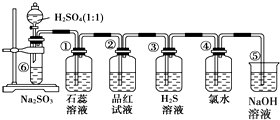 如图是实验室制备SO2并验证SO2某些性质的装置图,试回答:
如图是实验室制备SO2并验证SO2某些性质的装置图,试回答: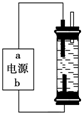 使用氯化钠作原料可以得到多种产品.
使用氯化钠作原料可以得到多种产品.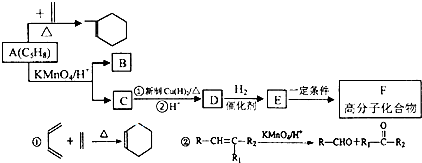
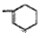 时,A发生的反应类型为
时,A发生的反应类型为