题目内容
15.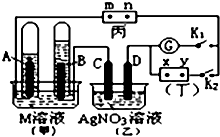 如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题:
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2:1,回答下列问题:(1)M溶液可能是A、B、C(填序号).
A.KNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液
D.NaCl溶液 E.CuSO4溶液
(2)C极的电极反应式为Ag++e-=Ag.
(3)滤纸丙的m端发生的现象为滤纸变蓝.
(4)闭合K2、断开K1一段时间后,断开K2、闭合K1,若M溶液为KOH溶液,则A极电极反应式为H2+2OH--2e-═2H2O.乙池电解质溶液的pH减小(填“增大”“减小”或“不变”).
分析 A、B两极产生的气体体积之比为2:1,则A电极上生成氢气,B电极上生成氧气,所以A为阴极,B为阳极,x为正极,y为负极;
(1)电解M的溶液实质上是电解水,结合选项分析;
(2)C与负极相连,为阴极,银离子得电子生成Ag;
(3)m与正极相连为阳极,碘离子失电子生成单质碘;
(4)闭合K2、断开K1一段时间后,断开K2、闭合K1,若M溶液为KOH溶液,甲中形成燃料电池,A上氢气失电子生成水;乙中为电解硝酸银溶液.
解答 解:A、B两极产生的气体体积之比为2:1,则A电极上生成氢气,B电极上生成氧气,所以A为阴极,B为阳极,x为正极,y为负极;
(1)电解KNO3溶液、Ba(OH)2溶液、H2SO4溶液实际上是电解水,电解氯化钠溶液是电解氯化钠和水,电解硫酸铜是电解铜离子和水,所以只有ABC符合;
故答案为:ABC;
(2)C与负极相连,为阴极,阴极上银离子得电子生成Ag,电极方程式为:Ag++e-=Ag;
故答案为:Ag++e-=Ag;
(3)m与正极相连为阳极,碘离子失电子生成单质碘,碘遇到淀粉会变蓝色,所以m端滤纸变蓝;
故答案为:滤纸变蓝;
(4)闭合K2、断开K1一段时间后,断开K2、闭合K1,若M溶液为KOH溶液,甲中形成燃料电池,A上氢气失电子生成水,则A的电极反应为:H2+2OH--2e-═2H2O;乙中为电解硝酸银溶液,反应为4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+,所以溶液的pH减小;
故答案为:H2+2OH--2e-═2H2O;减小.
点评 本题综合考查原电池和电解池知识,是高考中的常见题型和重要的考点之一,属于中等难度的试题,题目有利于培养学生分析问题、解决问题的能力,也有助于培养学生的逻辑思维能力和发散思维能力,注意根据电解现象判断阴阳极和正负极.

 阅读快车系列答案
阅读快车系列答案| A. | 硅是良好的半导体材料 | |
| B. | 氨气与硝酸合成氮肥属于人工固氮 | |
| C. | 金刚石、石墨和富勒烯互为同素异形体 | |
| D. | 硬铝、青铜和不锈钢都属于合金 |
I.实验需要90mL 0.10mol•L-1FeBr2溶液
(1)配制FeBr2溶液除烧杯、量筒、胶头滴管外还需的玻璃仪器是玻璃棒、100mL容量瓶.
(2)下列有关配制过程中说法错误的是abde(填序号).
a.用托盘天平称量质量为1.944g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II.探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色.某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+.
(3)请你完成下表,验证假设
| 实验步骤、预期现象 | 结论 |
| ①向溶液中加入四氯化碳,操作振荡、静置, 现象CCl4层呈橙红色,水层呈无色 | 假设1正确 |
| ②向溶液中另入KSCN溶液, 现象溶液变为红色 | 假设2正确 |
(4)若在50mL上述FeBr2溶液通入标准状况下112mL Cl2,反应的离子方程式为2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-.
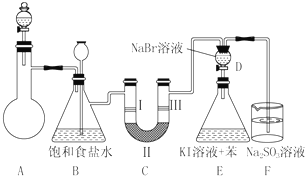
(1)制备氯气选用的药品为漂粉精固体和浓盐酸,相关反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是d(填编号).
| 编号 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.该现象不能(填“能”或“不能”)说明Br2的氧化性强于I2.
(4)有人提出,装置F中可改用过量的NaHSO3溶液吸收余氯,试写出相应反应的离子方程式4HSO3-+Cl2=SO42-+2Cl-+3SO2↑+2H2O;你认为不能(填“能”或“不能”)改用NaHSO3溶液.
| A. | 用敞开放置久了的浓硫酸进行配制 | B. | 量取浓硫酸仰视刻度线 | ||
| C. | 配制过程中未洗涤烧杯和玻璃棒 | D. | 配制前,容量瓶有少许蒸馏水 |
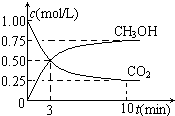 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.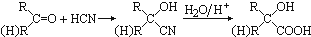 ,CO和H2按物质的量之比1:2可以制得G,有机玻璃可按下列路线合成:
,CO和H2按物质的量之比1:2可以制得G,有机玻璃可按下列路线合成: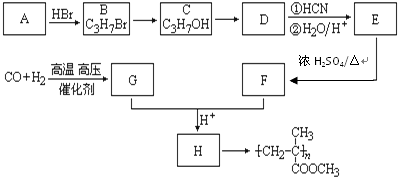
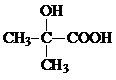 ;
; ;
;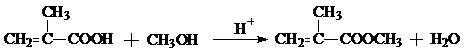 ;
; 氮可以形成多种化合物,如NH3、N2H4、HCN、NH4NO3等.
氮可以形成多种化合物,如NH3、N2H4、HCN、NH4NO3等.