题目内容
向Fe2(SO4)2和CuSO4的混合液中,加入足量的铁粉,充分反应后,过滤、洗涤、干燥,得地到固体沉淀质量与加入的铁粉质量相等,则原溶液Fe2(SO4)2和CuSO4溶液的物质的量浓度之比为多少?
考点:化学方程式的有关计算
专题:计算题
分析:向Fe2(SO4)3、CuSO4混和溶液中投入足量的铁粉,发生反应Fe+CuSO4=Cu+FeSO4,Fe+Fe2(SO4)3=3FeSO4,最后固体的质量与加入的铁粉的质量相等,则反应Fe+CuSO4=Cu+FeSO4导致固体增重等于反应Fe+Fe2(SO4)3=3FeSO4中参加反应的Fe的质量,假定反应Fe+Fe2(SO4)3=3FeSO4中参加反应的Fe的质量为56g,计算Fe2(SO4)3的物质的量,根据差量法计算CuSO4的物质的量,据此计算原溶液中Fe2(SO4)2和CuSO4溶液的物质的量浓度之比.
解答:
解:向Fe2(SO4)3、CuSO4混和溶液中投入足量的铁粉,发生反应Fe+CuSO4=Cu+FeSO4,Fe+Fe2(SO4)3=3FeSO4,最后固体的质量与加入的铁粉的质量相等,则反应Fe+CuSO4=Cu+FeSO4导致固体增重等于反应Fe+Fe2(SO4)3=3FeSO4中参加反应的Fe的质量,假定反应Fe+Fe2(SO4)3=3FeSO4中参加反应的Fe的质量为56g,物质的量为
=1mol,由方程式可知Fe2(SO4)3的物质的量为1mol,
Fe+CuSO4=Cu+FeSO4 固体增重△m
1mol 64g-56g=8g
n(CuSO4) 56g
故n(CuSO4)=
×1mol=7mol,
则在同一溶液中,Fe2(SO4)2和CuSO4溶液的物质的量浓度之比等于物质的量之比,即为1:7,
答:原溶液Fe2(SO4)2和CuSO4溶液的物质的量浓度之比为1:7.
| 56g |
| 56g/mol |
Fe+CuSO4=Cu+FeSO4 固体增重△m
1mol 64g-56g=8g
n(CuSO4) 56g
故n(CuSO4)=
| 56g |
| 8g |
则在同一溶液中,Fe2(SO4)2和CuSO4溶液的物质的量浓度之比等于物质的量之比,即为1:7,
答:原溶液Fe2(SO4)2和CuSO4溶液的物质的量浓度之比为1:7.
点评:本题考查混合物的有关计算,难度中等,根据方程式分析反应Fe+CuSO4=Cu+FeSO4导致固体增重等于反应Fe+Fe2(SO4)3=3FeSO4中参加反应的Fe的质量是解题的关键.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列有关化学用语的表述正确的是( )
A、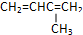 名称是3-甲基-1,3-丁二烯 名称是3-甲基-1,3-丁二烯 |
B、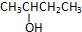 名称是2-羟基丁烷 名称是2-羟基丁烷 |
| C、二氧化碳的结构式:O=C=O |
D、乙烯的球棍模型: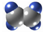 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O═CH3COOH+4H+.下列有关说法正确的是( )
| A、检测时,电解质溶液中的H+向负极移动 |
| B、电池反应的化学方程式为CH3CH2OH+O2═CH3COOH+H2O |
| C、正极上发生的反应为:O2+4e-+2H2O═4OH- |
| D、若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 |
如表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素.下列说法正确的是( )
| X | ||
| Y | Z | R |
| W |
| A、五种元素的原子最外层电子数一定都大于2 |
| B、X、Z原子序数可能相差18 |
| C、Z可能是氯元素 |
| D、Z的氧化物与X单质不可能发生置换反应 |
下列做法中不正确的是( )
| A、做喷泉实验来验证氨气极易溶解于水的性质 |
| B、金属钠着火时不可以用泡沫灭火器,可用干燥的沙土灭火 |
| C、用NaOH溶液除去混在CO2气体中的HCl |
| D、实验室中保存FeSO4溶液,应向其中加入铁粉 |