题目内容
11.下列说法中,不正确的是( )| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 禁止用工业酒精配制饮用酒和调味用的料酒 | |
| D. | 溴乙烷、TNT、葡萄糖都是无色溶于水的有机化合物 |
分析 A.乙醇与金属钠反应生成乙醇钠,断裂O-H键,生成氢气;
B.无水硫酸铜遇水变蓝色;
C.工业酒精中含有甲醇,有毒;
D.溴乙烷、TNT不溶于水.
解答 解:A.乙醇相当于水中的H原子被乙基取代生成的产物,与金属钠反应生成乙醇钠,断裂O-H键,生成氢气,故A正确;
B.无水硫酸铜遇水变蓝色,故可以利用无水硫酸铜检验乙醇中是否含有水分,故B正确;
C.工业酒精中含有甲醇,甲醇有毒,不能用于配制饮用酒和调味用的料酒,故C正确;
D.溴乙烷、TNT不溶于水,只有葡萄糖溶于水,故D错误.
故选D.
点评 本题主要考查常见有机化合物的性质,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,掌握常见有机物的官能团以及其在生活中的应用是关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列反应属于氧化还原反应的是( )
| A. | CaCO3+2HCl=CaCl2+H2O+CO2↑ | B. | Na2O+H2O=2NaOH | ||
| C. | CaCO3=CaO+CO2↑ | D. | Mg+2HCl=MgCl2+H2↑ |
19.下列叙述正确的是( )
| A. | Fe与S混合加热生成FeS2 | |
| B. | NaHCO3的热稳定性大于Na2CO3 | |
| C. | 铁与硝酸反应后溶液中一定有Fe3+存在 | |
| D. | Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
6.下列有关物质的性质和该性质的应用均正确的是( )
| A. | SiO2是酸性氧化物,可制成玻璃容器盛装氢氟酸 | |
| B. | 氧化铁为红棕色固体,可用于作油漆红色涂料 | |
| C. | 次氯酸有酸性,可用于自来水的杀菌消毒 | |
| D. | 钠具有金属活泼性,钠可以从硫酸铜溶液中置换出金属铜 |
3.下列有关化学用语表示不正确的是( )
| A. | 硝基苯的结构简式: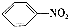 | B. | 氯化铵的电子式: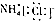 | ||
| C. | 甲烷的球棍模型: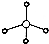 | D. | 乙醇的结构简式:CH3CH2OH |
20.下列各组中的离子,能再溶液中大量共存的是( )
| A. | H+、Na+、HCO3-、Cl- | B. | K+、Fe2+、Cl-、OH- | ||
| C. | Ag+、Al3+、NO3-、H+ | D. | Fe3+、Al3+、SCN-、Cl- |
1.下列有关实验操作错误的是( )
| A. | 用加热的方法区分纯碱和小苏打 | |
| B. | 用量筒量取5.0mL浓硫酸,并直接加水稀释 | |
| C. | 用分液漏斗分离苯和水的混合物 | |
| D. | 用托盘天平称量药品时,左盘放物品,右盘放砝码 |
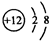 ;O的电子式为
;O的电子式为 ;H2S的结构式为H-S-H.
;H2S的结构式为H-S-H.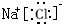 ,溶于水发生电离的电离方程式为NaCl=Na++Cl-,向氯化钠溶液中滴入硝酸银时发生反应的离子方程式为Ag++Cl-=AgCl↓.
,溶于水发生电离的电离方程式为NaCl=Na++Cl-,向氯化钠溶液中滴入硝酸银时发生反应的离子方程式为Ag++Cl-=AgCl↓.