题目内容
(共12分)现有下列种物质:① CH3OH
②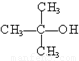
③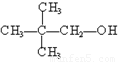 ④
④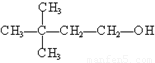 ⑤
⑤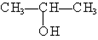
(1)能发生消去反应生成烯烃的是
(请填序号,下同),其消去产物依次是
;由此可以推出苯甲醇( ) (填“能”或“不能”)发生消去反应。
) (填“能”或“不能”)发生消去反应。
(2)能在铜的催化作用下,被空气中氧气氧化成醛的序号分别是 ,请写出能被氧化成酮的反应方程式:
【答案】
(1)②④⑤
(3分) 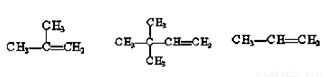 (3分)
(3分)
不能(1分)
(2)①③④
(3分)
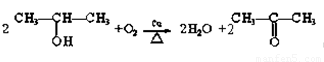 (2分)
(2分)
【解析】
试题分析:(1)醇发生消去反应时消去的是羟基和β-碳原子上的一个氢,所以①和③不能发生消去反应。
(2)醇被氧化首先去掉的是羟基上的氢和α-碳上的氢,从而形成碳氧双键。所以①③④氧化得到醛;②不能被氧化;⑤被氧化得到酮。
考点:考查醇的性质。

练习册系列答案
相关题目


