题目内容
下列离子方程式书写正确的是( )
| A、碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O |
| B、稀硫酸和氨水反应:H++NH3?H2O═NH4++H2O |
| C、氢氧化钠和硫酸反应:2OH-+H2SO4═SO42-+2H2O |
| D、铁钉放入硫酸铜溶液中:Fe+3Cu2+═2Fe3++3Cu |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钙属于难溶物写化学式;
B.一水合氨、水是弱电解质要写化学式,硫酸、硫酸铵是强电解质写离子;
C.硫酸是强电解质写离子;
D.二者发生置换反应生成硫酸亚铁和Cu.
B.一水合氨、水是弱电解质要写化学式,硫酸、硫酸铵是强电解质写离子;
C.硫酸是强电解质写离子;
D.二者发生置换反应生成硫酸亚铁和Cu.
解答:
解:A、碳酸钙为难溶物应用化学式,离子方程式为:CO32-+2H+=CO2↑+H2O,故A错误;
B、一水合氨、水是弱电解质要写化学式,硫酸、硫酸铵是强电解质写离子,离子方程式为:H++NH3?H2O=NH4++H2O,故B正确;
C、硫酸为可溶性强电解质,应拆成离子形式,离子方程式为:2OH-+H2SO4=SO42-+2H2O,故C错误;
D、二者发生置换反应生成硫酸亚铁和Cu,离子方程式为:Fe+Cu2+=Fe2++Cu,故D错误;
故选B.
B、一水合氨、水是弱电解质要写化学式,硫酸、硫酸铵是强电解质写离子,离子方程式为:H++NH3?H2O=NH4++H2O,故B正确;
C、硫酸为可溶性强电解质,应拆成离子形式,离子方程式为:2OH-+H2SO4=SO42-+2H2O,故C错误;
D、二者发生置换反应生成硫酸亚铁和Cu,离子方程式为:Fe+Cu2+=Fe2++Cu,故D错误;
故选B.
点评:本题考查离子方程式的书写,为高考高频点,明确物质的性质及离子方程式书写规则是解本题关键,注意要遵循客观事实、原子守恒、电荷守恒及转移电子守恒,易错选项是D.

练习册系列答案
 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
Rm+与Xn-具有相同的电子层结构,则微粒半径( )
| A、前者大于后者 |
| B、前者小于后者 |
| C、前者等于后者 |
| D、大小比较不能确定 |
下列属于阴离子的是( )
A、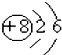 |
B、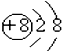 |
C、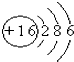 |
D、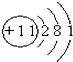 |
在下列溶液中,各组离子一定能够大量共存的是( )
| A、在含有NaHCO3的溶液中:K+、SO42-、Cl-、Al3+ |
| B、使甲基橙变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、水电离的c(H+)=10-11 mol?L-1的溶液:NH4+、K+、ClO-、Cl- |
能用H++OH-=H2O来表示的化学反应是( )
| A、氢氧化镁和稀盐酸反应 |
| B、Ba(OH)2溶液滴入稀硫酸中 |
| C、澄清石灰水和稀硝酸反应 |
| D、醋酸溶液与氢氧化钠溶液反应 |
下列各组离子,在指定的环境中一定能大量共存的是( )
| A、滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、SCN- |
| B、含 有大量HCO3-的溶液:NH4+、Ca2+、Mg2+、I- |
| C、c(S2-)=0.1 mol?L-1的溶液中:Na+、NH4+、ClO-、SO42- |
| D、含有大量ClO-的溶液:H+、Mg2+、I-、SO42- |
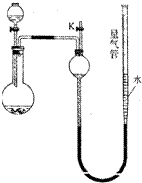 某同学设计如图所示装置(夹持装置已略去,量气管可上下移动)可分别进行下列实验探究
某同学设计如图所示装置(夹持装置已略去,量气管可上下移动)可分别进行下列实验探究