题目内容
能正确表示下列分应的离子方程式的是( )
A、实验室制氨气:NH4++OH-
| ||||
| B、向NaHCO3溶液中滴入少量澄清的石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | ||||
| C、酸性KMnO4溶液与H2O2反应:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | ||||
| D、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
考点:离子方程式的书写
专题:
分析:A.实验室用氯化铵固体和碱石灰共热制取氨气;
B.少量澄清石灰水和NaHCO3溶液溶液反应生成碳酸钙、碳酸钠和水;
C.酸性高锰酸钾和双氧水反应生成锰离子、氧气和水,其转移电子数为10;
D.醋酸是弱电解质,写化学式.
B.少量澄清石灰水和NaHCO3溶液溶液反应生成碳酸钙、碳酸钠和水;
C.酸性高锰酸钾和双氧水反应生成锰离子、氧气和水,其转移电子数为10;
D.醋酸是弱电解质,写化学式.
解答:
解:A.实验室用氯化铵固体和碱石灰共热制取氨气,该反应中没哟离子参加,所以没有离子方程式,故A错误;
B.少量澄清石灰水和NaHCO3溶液溶液反应生成碳酸钙、碳酸钠和水,离子方程式为2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O,故B正确;
C.酸性高锰酸钾和双氧水反应生成锰离子、氧气和水,其转移电子数为10,离子方程式为
2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故C错误;
D.醋酸是弱电解质,写化学式,离子方程式为CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故D错误;
故选B.
B.少量澄清石灰水和NaHCO3溶液溶液反应生成碳酸钙、碳酸钠和水,离子方程式为2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O,故B正确;
C.酸性高锰酸钾和双氧水反应生成锰离子、氧气和水,其转移电子数为10,离子方程式为
2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故C错误;
D.醋酸是弱电解质,写化学式,离子方程式为CaCO3+2CH3COOH═Ca2++H2O+CO2↑+2CH3COO-,故D错误;
故选B.
点评:本题考查离子方程式正误判断,为高考高频点,明确离子性质及离子反应条件即可解答,注意要遵循客观事实、原子守恒、电荷守恒及转移电子守恒,易错选项是BC,注意B中反应物的量不同其产物不同,为易错点.

练习册系列答案
相关题目
有下列离子的检验及其结论:①向某溶液中加入用盐酸酸化的BaCl2溶液,若产生白色沉淀,说明该溶液中含有SO42-②向某未知溶液中先加入几滴AgNO3溶液,再加入HNO3,若产生白色沉淀,说明未知溶液中含有Cl-③对某无色溶液进行焰色反应,观察到火焰呈黄色,说明该溶液含有Na+,但不能肯定是否含有K+.其中正确的是( )
| A、①②③ | B、①② | C、②③ | D、①③ |
下列离子方程式中,书写正确的是( )
| A、氢氧化钡溶液和稀硫酸反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| B、碳酸氢钠溶液与氢氧化钠溶液混合:HCO3-+OH-=CO32-+H2O |
| C、氧化亚铁溶于稀盐酸:O2-+2H+=H2O |
| D、稀盐酸滴到石灰石上:CO32-+2H+=CO2↑+H2O |
下列物质在空气中不能被酒精灯点燃的是( )
| A、钠块 | B、镁条 | C、铝箔 | D、硫粉 |

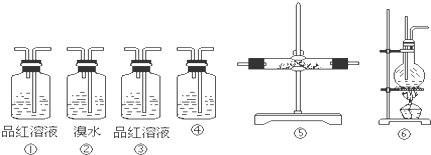

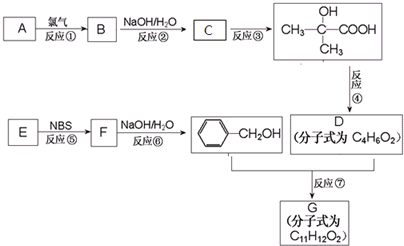
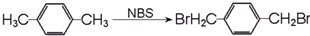
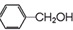 与
与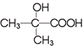 两种有机物,该试剂是
两种有机物,该试剂是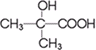 发生缩聚反应生成高分子化合物的结构简式
发生缩聚反应生成高分子化合物的结构简式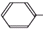 ;C、能使Br2的CCl4溶液褪色.
;C、能使Br2的CCl4溶液褪色.