题目内容
既能与盐酸反应,又能与氢氧化钠反应的有机物是( )
| A、CH3COOH |
| B、丙氨酸 |
| C、Al(OH)3 |
| D、NaHCO3 |
考点:镁、铝的重要化合物,两性氧化物和两性氢氧化物,氨基酸、蛋白质的结构和性质特点
专题:元素及其化合物,有机反应
分析:既能与盐酸反应又能与氢氧化钠溶液反应的物质有:两性化合物(如Al2O3、Al(OH)3等)、弱酸的酸式盐(NaHCO3、NaHS等)、弱酸的铵盐(如(NH4)2CO3等)、单质Al、氨基酸、蛋白质等.
解答:
解:A.CH3COOH与氢氧化钠溶液反应生成乙酸钠与水,不能与盐酸反应,故A错误;
B.丙氨酸属于氨基酸,既能与盐酸反应,又能和氢氧化钠溶液反应,故B正确;
C.Al(OH)3是两性氢氧化物,与盐酸反应生成氯化铝与水,与氢氧化钠溶液反应生成偏铝酸钠与水,但氢氧化铝不是有机物,故C错误;
D.NaHCO3是弱酸的酸式盐,与盐酸反应生成氯化钠、水和二氧化碳,与氢氧化钠溶液反应可以生成碳酸钠与水,但NaHCO3不是有机物,故D错误.
故选B.
B.丙氨酸属于氨基酸,既能与盐酸反应,又能和氢氧化钠溶液反应,故B正确;
C.Al(OH)3是两性氢氧化物,与盐酸反应生成氯化铝与水,与氢氧化钠溶液反应生成偏铝酸钠与水,但氢氧化铝不是有机物,故C错误;
D.NaHCO3是弱酸的酸式盐,与盐酸反应生成氯化钠、水和二氧化碳,与氢氧化钠溶液反应可以生成碳酸钠与水,但NaHCO3不是有机物,故D错误.
故选B.
点评:本题考查了元素化合物的性质,难度不大,注意归纳总结中学常见的既能与酸反应又能与碱反应的物质.

练习册系列答案
相关题目
某固体酸燃料电池以NaHSO4固体为电解质传递H+其基本结构见如图所示,电池总反应表示为:2H2+O2═2H2O下列有关说法正确的是( )


| A、电子通过外电路从b极流向a极 |
| B、H+由a极通过固体酸电解质传递到b极 |
| C、b极上的电极反应式为:O2+2H2O+4e-═4OH- |
| D、每转移0.1mol电子,消耗1.12L的H2 |
下列关于化学反应类型的叙述中,正确的是( )
| A、凡是生成盐和水的反应都是中和反应 |
| B、氧化还原反应一定有单质参加 |
| C、生成一种单质和一种化合物的反应一定是置换反应 |
| D、生成物中有单质的分解反应一定属于氧化还原反应 |
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如表所示,下列说法正确的是( )
| X | Y |
| Z | W |
| A、非金属性:Z<X<Y |
| B、W的原子序数可能是Y的原子序数的2倍 |
| C、气态氢化物稳定性:Y<W |
| D、四种元素中不可能有金属元素 |
下列说法正确的是( )
| A、液化气和天然气的主要成分都是甲烷 |
| B、油脂和羊毛都是高分子化合物 |
C、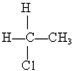 和 和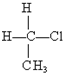 互为同分异构体 互为同分异构体 |
| D、由乙酸制乙酸乙酯的反应过程中,有取代反应发生 |
室温,在饱和澄清石灰水中加入CaO,待恢复到室温,测定溶液中各离子浓度( )
| A、pH值变大 |
| B、n (OH-)减少 |
| C、C (Ca2+)增大 |
| D、pH值减小 |
向100ml 2mol/L的AlCl3溶液中加入未知浓度的NaOH溶液100ml,产生7.8g沉淀.则此NaOH溶液的物质的量浓度可能是( )
| A、2mol/L |
| B、1.5mol/L |
| C、3mol/L |
| D、7mol/L |
分离氯化钠与氯化铵的混合物,采用以下哪种方法( )
| A、加水溶解法 | B、萃取法 |
| C、分液法 | D、加热法 |