题目内容
9.下列关于实验原理或操作的叙述不正确的是( )| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 利用重结晶可对粗苯甲酸进行提纯 | |
| C. | 不能用核磁共振氢谱来鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
分析 A.乙醇与水互溶,不能作萃取剂;
B.溶解度差异越大,利用重结晶分离效果越好;
C.1-溴丙烷中含3种H,2-溴丙烷中含2种H;
D.乙酸与CaO反应后,增大与乙醇的沸点差异.
解答 解:A.乙醇与水互溶,不能作萃取剂,则从碘水中提取单质碘时,不能用无水乙醇代替CCl4,故A正确;
B.溶解度差异越大,利用重结晶分离效果越好,则依据溶解度的差异,选择用重结晶的方法可将粗苯甲酸提纯,故B正确;
C.1-溴丙烷中含3种H,2-溴丙烷中含2种H,能用核磁共振氢谱来鉴别1-溴丙烷和2-溴丙烷,故C错误;
D.乙酸与CaO反应后,增大与乙醇的沸点差异,可采用先加生石灰,过滤后再蒸馏的方法提纯,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、物质鉴别等,把握物质的性质、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
20.某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Fe3+、Al3+、Clˉ.为确认该溶液组成进行如下实验:
①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
| A. | 一定含有Fe3+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Fe3+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c (Al3+)=1.00 mol•L-1 | |
| D. | c(Na+)=0.50 mol•L-1 |
17.25℃时,下列各组离子在指定溶液中一定能够大量共存的是( )
| A. | 0.1mol•L-1的A1Cl3溶液中:Na+、K+、CO32-、NO3- | |
| B. | pH=13的溶液中:Na+、NH4+、Cl-、NO3- | |
| C. | c(OH-)=1×10-13mol•L-1的溶液中:Mg2+、K+、Cl-、SO42- | |
| D. | 无色透明溶液中:Ca2-、NH4+、MnO4-、SO42- |
4.已知3X(g)+2Y(g)?nZ(g)+2W(g),若将0.6mol X和0.4mol Y混合充入一密闭体积可调的容器中,压强保持不变,5min后体积变为原来的1.2倍,则n值是( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
9.下列实验设计和结论相符的是( )
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定呈碱性 | |
| C. | 某无色溶液中加入BaCl2溶液,再加稀盐酸,沉淀不溶解,原溶液中一定有SO42- | |
| D. | 某无色溶液中加入酚酞试液变红,该溶液一定是碱溶液 |
7. 乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
①部分物质的沸点:
②乳酸乙酯易溶于苯、乙醇;
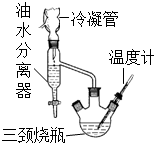
③水、乙醇、苯的混合物在64.85℃时,能按一定的比例以共沸物的形式一起蒸发.该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
第一步:在三颈烧瓶中加入0.1mol无水乳酸、过量的65.0mL无水乙醇、一定量的苯、沸石…;装上油水分离器和冷凝管,缓慢加热回流至反应完全.
第二步:将三颈烧瓶中液体倒入盛有过量某试剂的烧杯中,搅拌并分出有机相后,再用水洗.
第三步:将无水CaCl2加入到水洗后的产品中,过滤、蒸馏.
(1)第一步操作中,还缺少的试剂是浓硫酸;加入苯的目的是形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行;实验过程中,酯化反应进行完全的标志是油水分离器中液体不再增加.
(2)第二步中证明“水洗”已经完成的实验方案是测定水洗液的pH至7.
(3)利用核磁共振氢谱可以鉴定制备的产物是否为乳酸乙酯,乳酸乙酯分子核磁共振氢谱中有5个峰.
 乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精.为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:①部分物质的沸点:
| 物质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
③水、乙醇、苯的混合物在64.85℃时,能按一定的比例以共沸物的形式一起蒸发.该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
第一步:在三颈烧瓶中加入0.1mol无水乳酸、过量的65.0mL无水乙醇、一定量的苯、沸石…;装上油水分离器和冷凝管,缓慢加热回流至反应完全.
第二步:将三颈烧瓶中液体倒入盛有过量某试剂的烧杯中,搅拌并分出有机相后,再用水洗.
第三步:将无水CaCl2加入到水洗后的产品中,过滤、蒸馏.
(1)第一步操作中,还缺少的试剂是浓硫酸;加入苯的目的是形成水、乙醇、苯共沸物,分离反应生成的水,促进酯化反应正向进行;实验过程中,酯化反应进行完全的标志是油水分离器中液体不再增加.
(2)第二步中证明“水洗”已经完成的实验方案是测定水洗液的pH至7.
(3)利用核磁共振氢谱可以鉴定制备的产物是否为乳酸乙酯,乳酸乙酯分子核磁共振氢谱中有5个峰.
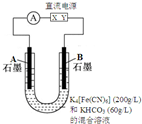 气态废弃物中的硫化氢可用下法转化为可利用的硫.
气态废弃物中的硫化氢可用下法转化为可利用的硫.