题目内容
A、B、C、D、E、F是元素周期表前四周期的六种元素,原子序数依次增大,其相关信息如下表:
(1)C位于元素周期表第 周期第 族.F元素基态原子的核外电子排布式是 .
(2)六种元素中,电负性最大的元素是 (填元素符号),D的一种核素原子核内有10个中子,该核素的符号是 .
(3)E2D2的电子式是 ,BD2的晶体类型为 .化合物丙由D、F两种元素组成,丙可作油漆的一种颜料,化合物丁由B、D两种元素组成.工业上由丙和丁在高温下反应生产F的单质,写出该反应的化学方程式: .
(4)在2L密闭容器中加入3molA2和一定量C2发生反应:3A2+C2?2CA3△H<0,反应10min达到平衡,生成0.2mol CA3.
①该反应平衡常数表达式为(各物质均写化学式)K= .
②从起始到平衡,以C2浓度变化表示的平均反应速率为 .
| 元素 | 相关信息 |
| A | 原子的核外电子数和电子层数相等 |
| B | 基态原子价电子排布为nsnnpn |
| C | 气态氢化物与最高价氧化物的水化物反应生成盐 |
| D | 基态原子电子排布有2个未成对电子 |
| E | 位于第三周期,在同周期中原子半径最大 |
| F | 与B 形成的合金为目前用量最多的金属材料 |
(2)六种元素中,电负性最大的元素是
(3)E2D2的电子式是
(4)在2L密闭容器中加入3molA2和一定量C2发生反应:3A2+C2?2CA3△H<0,反应10min达到平衡,生成0.2mol CA3.
①该反应平衡常数表达式为(各物质均写化学式)K=
②从起始到平衡,以C2浓度变化表示的平均反应速率为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A的原子的核外电子数和电子层数相等,则A为H元素;
B的基态原子价电子排布为nsnnpn,s轨道含有2个电子,则n=2,其基态原子价电子排布为2s22p2,则B为C元素;
C的气态氢化物与最高价氧化物的水化物反应生成盐,说明C的氢化物学生碱性,则C为N元素;
D的基态原子电子排布有2个未成对电子,结合原子序数依次增大,E为钠,则D位于第2周期,原子序数大于7,则D的外围电子排布为2s22p4,即D为O;
E位于第三周期,在同周期中原子半径最大,则D为第三周期ⅠA族元素,即D为Na元素;
F与铁元素形成的合金为目前用量最多的金属材料,则该合金为钢,F为Fe元素,
根据以上分析进行解答.
B的基态原子价电子排布为nsnnpn,s轨道含有2个电子,则n=2,其基态原子价电子排布为2s22p2,则B为C元素;
C的气态氢化物与最高价氧化物的水化物反应生成盐,说明C的氢化物学生碱性,则C为N元素;
D的基态原子电子排布有2个未成对电子,结合原子序数依次增大,E为钠,则D位于第2周期,原子序数大于7,则D的外围电子排布为2s22p4,即D为O;
E位于第三周期,在同周期中原子半径最大,则D为第三周期ⅠA族元素,即D为Na元素;
F与铁元素形成的合金为目前用量最多的金属材料,则该合金为钢,F为Fe元素,
根据以上分析进行解答.
解答:
解:A的原子的核外电子数和电子层数相等,则A为H元素;
B的基态原子价电子排布为nsnnpn,s轨道含有2个电子,则n=2,其基态原子价电子排布为2s22p2,则B为C元素;
C的气态氢化物与最高价氧化物的水化物反应生成盐,说明C的氢化物学生碱性,则C为N元素;
D的基态原子电子排布有2个未成对电子,结合原子序数依次增大,E为钠,则D位于第2周期,原子序数大于7,则D的外围电子排布为2s22p4,即D为O;
E位于第三周期,在同周期中原子半径最大,则E为第三周期ⅠA族元素,即E为Na元素;
F与铁元素形成的合金为目前用量最多的金属材料,则该合金为钢,F为Fe元素,
(1)C为N元素,位于元素周期表第二周ⅤA族;F为Fe元素,Fe是26元素,核外电子数为26,态原子的核外电子排布式为:1s22s22p63s23p63d64s2,
故答案为:二;ⅤA;1s22s22p63s23p63d64s2;
(2)以上6种元素中,O的非金属性最强,电负性最大;O的一种核素原子核内有10个中子,其质量数为18,该核素的符号是:818O,
故答案为:O;818O;
(3)E为Na元素、D为O,E2D2为Na2O2,过氧化钠属于离子化合物,由钠离子与过氧根离子构成,电子式为: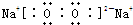 ;
;
B为C元素,BD2为CO2,二氧化碳的晶体为分子晶体;
化合物丙由D、F两种元素组成,丙可作油漆的一种颜料,则丙为氧化铁,化合物丁由B、D两种元素组成,工业上由丙和丁在高温下反应生产F的单质,则丁为CO,该反应的化学方程式为:3CO+Fe2O3
2Fe+3CO2,
故答案为: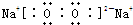 ;分子;3CO+Fe2O3
;分子;3CO+Fe2O3
2Fe+3CO2;
(4)A为H元素,C为N元素,则A2为H2,C2为N2,反应方程式为:3H2+N2?2NH3,
①反应3H2+N2?2NH3的平衡常数表达式为:K=
,
故答案为:
;
②3molH2和一定量N2发生反应,反应10min达到平衡,生成0.2mol NH3,则10min内氨气的平均反应速率为:v(NH3)=
=0.01mol/(L?min),
反应速率与化学计量数成正比,则从起始到平衡,以N2浓度变化表示的平均反应速率为:v(N2)=
v(NH3)=0.005mol/(L?min),
故答案为:0.005mol/(L?min).
B的基态原子价电子排布为nsnnpn,s轨道含有2个电子,则n=2,其基态原子价电子排布为2s22p2,则B为C元素;
C的气态氢化物与最高价氧化物的水化物反应生成盐,说明C的氢化物学生碱性,则C为N元素;
D的基态原子电子排布有2个未成对电子,结合原子序数依次增大,E为钠,则D位于第2周期,原子序数大于7,则D的外围电子排布为2s22p4,即D为O;
E位于第三周期,在同周期中原子半径最大,则E为第三周期ⅠA族元素,即E为Na元素;
F与铁元素形成的合金为目前用量最多的金属材料,则该合金为钢,F为Fe元素,
(1)C为N元素,位于元素周期表第二周ⅤA族;F为Fe元素,Fe是26元素,核外电子数为26,态原子的核外电子排布式为:1s22s22p63s23p63d64s2,
故答案为:二;ⅤA;1s22s22p63s23p63d64s2;
(2)以上6种元素中,O的非金属性最强,电负性最大;O的一种核素原子核内有10个中子,其质量数为18,该核素的符号是:818O,
故答案为:O;818O;
(3)E为Na元素、D为O,E2D2为Na2O2,过氧化钠属于离子化合物,由钠离子与过氧根离子构成,电子式为:
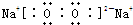 ;
;B为C元素,BD2为CO2,二氧化碳的晶体为分子晶体;
化合物丙由D、F两种元素组成,丙可作油漆的一种颜料,则丙为氧化铁,化合物丁由B、D两种元素组成,工业上由丙和丁在高温下反应生产F的单质,则丁为CO,该反应的化学方程式为:3CO+Fe2O3
| ||
故答案为:
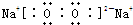 ;分子;3CO+Fe2O3
;分子;3CO+Fe2O3
| ||
(4)A为H元素,C为N元素,则A2为H2,C2为N2,反应方程式为:3H2+N2?2NH3,
①反应3H2+N2?2NH3的平衡常数表达式为:K=
| c2(NH3) |
| c3(H2)?c(N2) |
故答案为:
| c2(NH3) |
| c3(H2)?c(N2) |
②3molH2和一定量N2发生反应,反应10min达到平衡,生成0.2mol NH3,则10min内氨气的平均反应速率为:v(NH3)=
| ||
| 10min |
反应速率与化学计量数成正比,则从起始到平衡,以N2浓度变化表示的平均反应速率为:v(N2)=
| 1 |
| 2 |
故答案为:0.005mol/(L?min).
点评:本题考查了物质、结构与性质的综合应用、化学反应速率的计算、化学平衡常数的书写等知识,题目难度中等,根据题干信息正确分析各元素名称为解答关键,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
已知部分被氧化的镁条1.6g和足量的盐酸反应,在标准状况下生成了H2 1.12L,在跟盐酸反应前被氧化的镁是( )
| A、0.24g | B、0.64g |
| C、0.4g | D、1.2g |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使紫色石蕊试剂显红色的溶液:NH4+、K+、[Al(OH)4]-、NO3- |
| B、稀HNO3溶液:Na+、Mg2+、SO42-、Cl- |
| C、FeCl3溶液:K+、Na+、I-、SO42- |
| D、由水电离产生的c(H+)=10-13 mol?L-1的溶液:K+、Na+、Cl-、HCO3- |
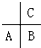 短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )
短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )| A、若均为非金属元素,其气态氢化物稳定性:A<B<C |
| B、若均为金属元素,其最高价氧化物的水化物的碱性:A<B<C |
| C、原子半径:A>C>B |
| D、最高正价:A>B>C |
2007年10月24日,我国自行研发的第一颗探月卫星“嫦娥一号”顺利升空.“嫦娥一号”的主要任务之一是探明月球上
He量.据科学家预测,月球的土壤中吸附着数百万吨的
He,每百吨
He核聚变所释放出的能量相当于目前人类一年消耗的能量.下列关于
He的说法中,不正确的是( )
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| A、中子数为1 |
| B、质子数为2 |
| C、质量数为3 |
D、原子结构示意图是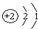 |
某有机物的结构为HO-CH2-CH=CHCH2-COOH,该有机物不可能发生的化学反应是( )
| A、水解反应 | B、酯化反应 |
| C、加成反应 | D、氧化反应 |
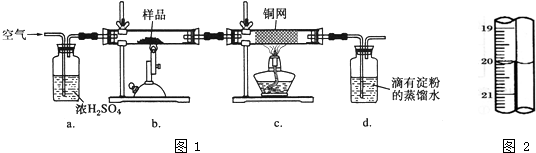
 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制200mL 1.0mol/L的稀硫酸.可供选用的仪器有:
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制200mL 1.0mol/L的稀硫酸.可供选用的仪器有: