题目内容
硝酸铵(NH4NO3)在不同条件下分解可得到不同的产物,下列各组物质中肯定不可能是硝酸铵分解产物的是( )
| A、HNO3、NO、H2O |
| B、N2、HNO3、H2O |
| C、N2、O2、H2O |
| D、N2O、H2O |
考点:铵盐
专题:氮族元素
分析:依据反应过程中元素化合价有升有降,且化合价变化时电子守恒分析产物.
解答:
解:A、NH4NO3分解过程中,若生成HNO3、NO、H2O,氮元素化合价升高-3价变化为+2价,变化5价,化合价降低,+5价变化为+2价,变化3价,化学式分析判断,元素化合价变化不相同,不能遵循电子守恒,故A错误;
B、NH4NO3分解过程中,若生成N2、HNO3、H2O,氮元素化合价-3价变化为0价,+5价变化为0价,该分子中铵根离子中的氮原子失电子,一个铵根离子失去3个电子生成氮原子,硝酸根离子中的氮原子得电子,一个硝酸根离子得到5个电子生成氮原子,其最小公倍数是15,所以其反应方程式为5NH4NO3=4N2+2HNO3+9H2O,故B正确;
C、NH4NO3分解过程中,若生成N2、O2、H2O,氮元素化合价-3价、+5价变化为0价,氧元素化合价-2价变化为0价,反应的化学方程式为2NH4NO3=2N2+O2+4H2O,可以符合电子守恒,故C正确;
D、NH4NO3分解过程中,若生成N2O、H2O,氮元素化合价-3价变化为+1价,+5价变化为+1价,依据化学式分析化学方程式为NH4NO3=N2O+2H2O符合电子守恒,故D正确;
故选A.
B、NH4NO3分解过程中,若生成N2、HNO3、H2O,氮元素化合价-3价变化为0价,+5价变化为0价,该分子中铵根离子中的氮原子失电子,一个铵根离子失去3个电子生成氮原子,硝酸根离子中的氮原子得电子,一个硝酸根离子得到5个电子生成氮原子,其最小公倍数是15,所以其反应方程式为5NH4NO3=4N2+2HNO3+9H2O,故B正确;
C、NH4NO3分解过程中,若生成N2、O2、H2O,氮元素化合价-3价、+5价变化为0价,氧元素化合价-2价变化为0价,反应的化学方程式为2NH4NO3=2N2+O2+4H2O,可以符合电子守恒,故C正确;
D、NH4NO3分解过程中,若生成N2O、H2O,氮元素化合价-3价变化为+1价,+5价变化为+1价,依据化学式分析化学方程式为NH4NO3=N2O+2H2O符合电子守恒,故D正确;
故选A.
点评:本题考查了氧化还原反应产物分析判断,元素化合价变化和化学式组成特征,掌握元素化合价变化特征分析方法是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在 2H2S+SO2═3S↓+2H2O 的反应中,被还原的元素是( )
| A、硫元素 | ||
| B、H2S中的硫元素 | ||
C、
| ||
D、
|
下列措施肯定能使反应速率增大的是( )
| A、增大反应物的量 |
| B、增大压强 |
| C、适当升高温度 |
| D、降低反应物浓度 |
相同质量的下列各烃,完全燃烧后生成水最多的是( )
| A、甲烷 | B、乙烷 | C、乙烯 | D、乙炔 |
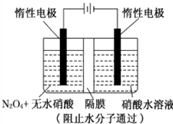 如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )
如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )| A、阴极的电极反应为:NO3-+4H++3e-=NO↑+2H2O |
| B、阳极的电极反应为:N2O4+2 HNO3-2e-=2N2O5+2H+ |
| C、当电路中通过6 mol e-时整个电解池中参与反应的HNO3为8mol |
| D、当电路中通过6 mol e-时,有8molH+从阳极向阴极迁移 |
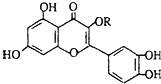 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P 的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P 的叙述错误的是( )| A、可以和溴水反应 |
| B、可用有机溶剂萃取 |
| C、分子中有二个苯环 |
| D、1mol维生素P可以和3molNaOH反应 |
下列说法正确的是( )
| A、凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B、自发反应在恰当条件下才能实现 |
| C、自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| D、自发反应在任何条件下都能实现 |
生活中常见的三种物质:①柠檬汁,②肥皂水,③食盐水,按溶液pH由小到大排列正确的是( )
| A、①②③ | B、.①③② |
| C、.③②① | D、.②①③ |
下列方法不可用于鉴别甲烷和乙烯两种气体的是( )
| A、点燃 |
| B、气体通入溴的四氯化碳溶液 |
| C、气体通过酸性高锰酸钾溶液 |
| D、气体通入氢氧化钠溶液 |