题目内容
6.有X、Y、Z三种元素:(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
(5)Z单质溶于X2Y中,所得溶液具有漂白性.
试写出其元素符号:XH,YO,ZCl,以及化合物的分子式:XZHCl,X2YH2O.
分析 有X、Y、Z三种元素:(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色,说明是氢气在氯气中燃烧生成氯化氢,X为H2,Z为Cl2,生成XZ为HCl;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红,说明Z是HCl,溶于水形成盐酸溶液;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体判断为H2O,所以Y为O;
(5)Z单质溶于X2Y中所得溶液具有漂白性,是Cl2溶于H2O中反应生成HCl和HClO,HClO具有漂白作用,据此进行解答.
解答 解:有X、Y、Z三种元素:(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色,说明是氢气在氯气中燃烧生成氯化氢,X为H2,Z为Cl2,生成XZ为HCl;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红,说明Z是HCl,溶于水形成盐酸溶液;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体判断为H2O,所以Y为O;
(5)Z单质溶于X2Y中所得溶液具有漂白性,是Cl2溶于H2O中反应生成HCl和HClO,HClO具有漂白作用,
根据分析可知,X为H,Y为O,Z为Cl,XZ为HCl,X2Y为H2O,
故答案为:H;O;Cl;HCl;H2O.
点评 本题考查位置结构与性质关系的综合应用,题目难度不大,注意根据物质的颜色、状态作为推断的突破口,旨在考查学生对基础知识的积累与熟练程度.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
19.三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,Cu2O在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是固体完全溶解,溶液呈血红色.
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色.
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是Fe2O3和Cu2O,写出发生反应的离子方程式Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+.
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾 (CuSO4•5H2O)经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
实验室有下列试剂可供选择:
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:
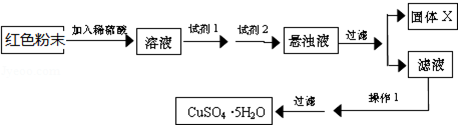
试回答:①试剂I为B,试剂II为F(填字母).
②固体X的化学式为Fe(OH)3.
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,Cu2O在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是固体完全溶解,溶液呈血红色.
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?不合理;当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色.
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是Fe2O3和Cu2O,写出发生反应的离子方程式Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+.
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为$\frac{9(b-a)}{a}$×100%.
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾 (CuSO4•5H2O)经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
A.氯水 B.H2O2 C.硝酸 D.NaOH E.氨水 F.Cu2(OH)2CO3
实验小组设计如下实验方案:

试回答:①试剂I为B,试剂II为F(填字母).
②固体X的化学式为Fe(OH)3.
20.下列粒子在化学反应中容易得到电子的是( )
| A. | 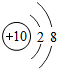 | B. |  | C. | 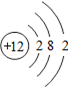 | D. | 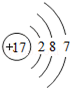 |
17.改变某一条件使NH4Cl稀溶液中NH4+的数目增加,下列说法正确的是( )
| A. | 此时溶液可能为中性 | |
| B. | 此时溶液中NH4+的浓度一定增大 | |
| C. | 此时NH4+的水解程度一定增大 | |
| D. | 此过程中,溶液中NH3•H2O和NH4+的数目之和一定增大 |
1.一包混有杂质的碳酸钠固体,其杂质可能是Ba(NO3)2、KCl及NaHCO3中的一种或两种.今取样品溶于适量水得到澄清溶液.另取10.6克该固体样品跟足量的盐酸反应收集到4.4克二氧化碳,则下列判断中正确的是( )
| A. | 样品中只含一种杂质NaHCO3 | B. | 样品中含有KCl,不含有NaHCO3 | ||
| C. | 样品中含有Ba(NO3)2和NaHCO3 | D. | 样品中含有KCl和NaHCO3 |
11.化学与环境、材料、信息、能源关系密切,下列说法中不正确的是( )
| A. | 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水 | |
| B. | “光化学烟雾”、“臭氧空洞”的形成都与氮氧化合物有关 | |
| C. | 使用含12C的产品,减少使用含13C或14C的产品符合“促进低碳经济”宗旨 | |
| D. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
15.已知在298K时下述反应的有关数据如下:
C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1则C(s)+CO2(g)═2CO(g)的△H为( )
C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1则C(s)+CO2(g)═2CO(g)的△H为( )
| A. | +283.5 kJ•mol-1 | B. | -172.5 kJ•mol-1 | C. | +172.5 kJ•mol-1 | D. | -504 kJ•mol-1 |