题目内容
下列有关离子方程式或热化学方程式书写正确的是( )
| A、石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ | ||||
B、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、将碳与足量的浓硫酸共热反应后的气体混合物,通入过量氢氧化钠溶液中:CO2+SO2+4OH-=SO32+CO32-+2H2O | ||||
| D、84消毒液和洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+=Cl2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.石灰乳写化学式;
B.生成的氢氧根离子和镁离子反应生成氢氧化镁沉淀;
C.二者反应生成亚硫酸钠和碳酸钠;
D.二者反应生成氯气和水.
B.生成的氢氧根离子和镁离子反应生成氢氧化镁沉淀;
C.二者反应生成亚硫酸钠和碳酸钠;
D.二者反应生成氯气和水.
解答:
解:A.石灰乳写化学式,离子方程式为Ca(OH)2+CO32-=CaCO3↓+2OH-,故A错误;
B.生成的氢氧根离子和镁离子反应生成氢氧化镁沉淀,离子方程式为Mg2++2Cl-+2H2O
Cl2↑+Mg(OH)2↓+H2↑,故B错误;
C.二者反应生成亚硫酸钠和碳酸钠和水,离子方程式为CO2+2SO2+6OH-=2SO32-+CO32-+3H2O,故C错误;
D.二者反应生成氯气和水,离子方程式为Cl-+ClO-+2H+=Cl2↑+H2O,故D正确;
故选D.
B.生成的氢氧根离子和镁离子反应生成氢氧化镁沉淀,离子方程式为Mg2++2Cl-+2H2O
| ||
C.二者反应生成亚硫酸钠和碳酸钠和水,离子方程式为CO2+2SO2+6OH-=2SO32-+CO32-+3H2O,故C错误;
D.二者反应生成氯气和水,离子方程式为Cl-+ClO-+2H+=Cl2↑+H2O,故D正确;
故选D.
点评:本题考查离子方程式正误判断,明确物质的性质、离子反应概念、离子反应书写规则即可解答,单质、氧化物、气体、沉淀、弱电解质、络合物都写化学式,注意A中石灰乳写化学式,注意B中镁离子在碱性溶液中不能存在,这些都是易错点.

练习册系列答案
相关题目
下列关于仪器使用的说法正确的是( )
| A、滴定管装滴定液时应先用滴定液润洗 |
| B、锥形瓶用作反应容器时一定不能加热 |
| C、蒸馏时温度计水银球可以高于蒸馏瓶支管口 |
| D、萃取时振荡分液漏斗应关闭其玻璃塞并打开活塞 |
已知还原性由强到弱的顺序是:S2-、I-、Br-,向含有上述阴离子的溶液中Cl2(上述三种阴离子均能被Cl2氧化为单质).则下列判断正确的是( )
| A、.先有S生成 |
| B、.先有I2生成 |
| C、.先有Br2生成 |
| D、.以上结论均不正确 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
| B、2g氢气所含分子数目为2NA |
| C、在标准状况下,以任意比混合的氦气和氧气混合物22.4L,所含分子数为NA |
| D、在25℃、101kPa时,11.2L氮气所含的原子数目为NA |
能正确表示下列反应的离子方程式是( )
| A、向KHSO4溶液中加入Ba(OH)2溶液至所得溶液呈中性Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、向Ca(HCO3)2溶液中滴入过量的NaOH溶液Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
溶液和胶体的本质区别在于( )
| A、分散质微粒直径大小不同 |
| B、是否均一、稳定 |
| C、是否能发生丁达尔效应 |
| D、是否透明 |
德国人弗里茨?哈伯(Fritz Haber)由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量.下列说法中正确的是( )
| A、N2和H2在点燃或光照条件下可合成氨 |
| B、氨是共价化合物,硝酸是离子化合物 |
| C、氨气遇到浓硝酸会发生反应产生白烟 |
| D、由氨制取硝酸过程中,氮元素被还原 |
可逆反应2A(g)+3B(g)?2C(g);△H=-QkJ?mol-1(Q>0).现有甲、乙两个容积相同且不变的真空密闭容器,向甲容器中加入2molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2 kJ;已知2Q1=Q2.下列叙述正确的( )
| A、平衡时甲、乙中C的体积分数甲>乙 |
| B、平衡时甲中A的转化率为60% |
| C、达到平衡后,再向乙中加入0.8molA+1.2molB+1.2molC,平衡向生成A的正向移动 |
| D、D甲容器达到平衡后,升温,反应的平衡常数增大 |
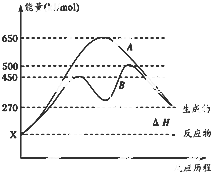 (1)已知:①Fe(s)+
(1)已知:①Fe(s)+