题目内容
为测定Na2CO3 、NaCl和NaBr组成的混合物中各物质的质量分数,进行如下实验:
(1)取9.00g混合物加入足量的盐酸,产生0.448LCO2 (S.T.P)
(2)在上述溶液中滴入足量的氯气,待完全反应后将溶液蒸干,称得固体的质量为8.775g,求Na2CO3 、NaCl和NaBr的质量分数分别为多少?
(1)取9.00g混合物加入足量的盐酸,产生0.448LCO2 (S.T.P)
(2)在上述溶液中滴入足量的氯气,待完全反应后将溶液蒸干,称得固体的质量为8.775g,求Na2CO3 、NaCl和NaBr的质量分数分别为多少?
考点:有关混合物反应的计算
专题:计算题
分析:碳酸钠与盐酸反应生成二氧化碳,根据碳元素守恒计算碳酸钠的质量,反应后溶液中滴入足量的氯气,发生反应:2NaBr+Cl2=2NaCl+Br2,溴在加热过程中易挥发,将溶液蒸干称得固体的质量为4.33g为NaCl的质量(包含原混合物中NaCl、反应生成的NaCl),设原混合物中NaCl、NaBr的物质的量分别为xmol、ymol,根据钠离子守恒与混合物总质量列方程计算原混合物中NaCl、NaBr的物质的量,进而计算原混合物各组分的质量分数.
解答:
解:碳酸钠与盐酸反应产生0.448LCO2 ,n(CO2 )=
=0.02mol,根据碳元素守恒,n(Na2CO3)=n(CO2 )=0.02mol,则m(Na2CO3)=0.02mol×106g/mol=2.12g,故w(Na2CO3)=
×100%=23.56%;
原混合物中NaCl与NaBr的质量为9g-2.12g=6.88g,
反应后溶液中滴入足量的氯气,发生反应:2NaBr+Cl2=2NaCl+Br2,溴在加热过程中易挥发,将溶液蒸干称得固体的质量为8.775g为NaCl的质量(包含原混合物中NaCl、反应生成的NaCl),其物质的量为
=0.15mol,设原混合物中NaCl、NaBr的物质的量分别为xmol、ymol,根据钠离子守恒与二者总质量,则:
解得x=0.1 y=0.01,
故原混合物中NaCl的质量为0.1mol×58.5g/mol=5.85g,其质量分数为
×100%=65%;
原混合物中NaBr的质量为0.01mol×103g/mol=1.03g,其质量分数为
×100%=11.44%,
答:原混合物质碳酸钠的质量分数为23.56%,NaCl质量分数为65%,NaBr的质量分数为11.44%.
| 0.448L |
| 22.4L/mol |
| 2.12g |
| 9g |
原混合物中NaCl与NaBr的质量为9g-2.12g=6.88g,
反应后溶液中滴入足量的氯气,发生反应:2NaBr+Cl2=2NaCl+Br2,溴在加热过程中易挥发,将溶液蒸干称得固体的质量为8.775g为NaCl的质量(包含原混合物中NaCl、反应生成的NaCl),其物质的量为
| 8.775g |
| 58.5g/mol |
|
解得x=0.1 y=0.01,
故原混合物中NaCl的质量为0.1mol×58.5g/mol=5.85g,其质量分数为
| 5.85g |
| 9g |
原混合物中NaBr的质量为0.01mol×103g/mol=1.03g,其质量分数为
| 1.03g |
| 9g |
答:原混合物质碳酸钠的质量分数为23.56%,NaCl质量分数为65%,NaBr的质量分数为11.44%.
点评:本题考查混合物计算,注意利用守恒法解答,侧重考查学生的分析计算能力,难度中等.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4 L CHCl3中含有的氯原子数目为3NA |
| B、7 g CnH2n中含有的氢原子数目为NA |
| C、18 g D2O中含有的质子数目为10 NA |
| D、1 L 0.5 mol?L-1Na2CO3溶液中含有的CO32-数目为0.5 NA |
若1mol 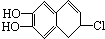 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )
 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是( )| A、1mol、2mol |
| B、2mol、3mol |
| C、3mol、2mol |
| D、3mol、3mol |
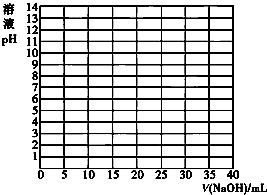 酸碱中和滴定常用于测定酸碱溶液的浓度.
酸碱中和滴定常用于测定酸碱溶液的浓度.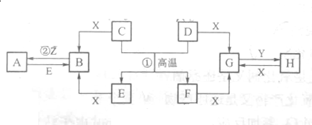 已知D、E、Z是单质,其他都是化合物.D既能与强酸反应,又能与强碱反应;潮湿的Z有漂白性;Y的焰色反应显黄色.除反应①外,其他反应均在水溶液中进行,转化关系如图所示(部分物质条件已略去).
已知D、E、Z是单质,其他都是化合物.D既能与强酸反应,又能与强碱反应;潮湿的Z有漂白性;Y的焰色反应显黄色.除反应①外,其他反应均在水溶液中进行,转化关系如图所示(部分物质条件已略去).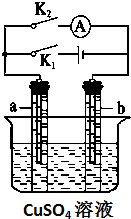 如图所示,某同学按照图装置进行如下实验,请回答下列问题:
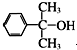
如图所示,某同学按照图装置进行如下实验,请回答下列问题: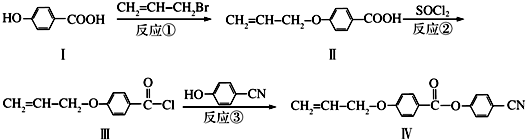
 也可与Ⅲ发生类似反应③的反应生成有机物V.V的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物V.V的结构简式是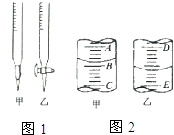 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空: