题目内容
4.下列物质不属于危险品的是( )| A. | 硝化甘油 | B. | 苯 | C. | 重晶石 | D. | 硝酸铵 |
分析 易燃物、易爆物、腐蚀品都属于危险品,据此解题.
解答 解:A.硝化甘油是易爆品,易发生爆炸,故A错误;
B.苯是易燃物,故B错误;
C.重晶石性质稳定,不属于危险品,故C正确;
D.硝酸铵是易爆品,易发生爆炸,故D错误.
故选C.
点评 本题考查危险品,难度不大,注意了解生活中常见的易燃物、易爆物、腐蚀品和危险品等,将安全问题放在心上.

练习册系列答案
相关题目
14.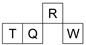 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 原子半径:T>Q>R | |
| C. | 最高价氧化物对应水化物的酸性:Q<W | |
| D. | 含T元素的盐溶液一定显酸性 |
15.能证明BF3为平面三角形而不是三角锥形分子的理由是( )
| A. | BF2Cl只有一种结构 | B. | 三根B-F键间键角都为120° | ||
| C. | BFCl2只有一种结构 | D. | 三根B-F键键长都为130pm |
12. 如图是某同学研究铜与浓硫酸的反应装置:
如图是某同学研究铜与浓硫酸的反应装置:
完成下列填空:
(1)写出A中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
采用可抽动铜丝进行实验的优点是可以控制反应的进行.
(2)反应一段时间后,可观察到B试管中的现象为变红.
(3)从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是NH3、
Cl2.(要求填一种化合物和一种单质的化学式)
(4)反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是过滤.该黑色不溶物不可能是CuO,理由是CuO会溶于稀硫酸中.
(5)对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:
①根据实验现象可判断黑色不溶物中一定含有硫元素.
②若该黑色不溶物由两种元素组成且在反应前后质量保持不变,推测其化学式为Cu2S.
 如图是某同学研究铜与浓硫酸的反应装置:
如图是某同学研究铜与浓硫酸的反应装置:完成下列填空:
(1)写出A中发生反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
采用可抽动铜丝进行实验的优点是可以控制反应的进行.
(2)反应一段时间后,可观察到B试管中的现象为变红.
(3)从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是NH3、
Cl2.(要求填一种化合物和一种单质的化学式)
(4)反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是过滤.该黑色不溶物不可能是CuO,理由是CuO会溶于稀硫酸中.
(5)对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:
| 实验装置 | 实验现象 |
 | 品红褪色 |
②若该黑色不溶物由两种元素组成且在反应前后质量保持不变,推测其化学式为Cu2S.
19.下列实验现象,解释或结论正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中龠Na+,不含K+ |
| B | 向某溶液中滴加KSCN溶液,无明显现象,再滴加 少量氯水,溶液变成红色 | 溶液中含有Fe2+,没有Fe3+ |
| C | 向苯中滴入少量浓溴水,振荡,精置分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 在少量无水乙醇中加入金属Na+,缓慢生成可以在空气中燃烧的气体 | CH3CH2OH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
9.下列操作不正确的是( )
| A. | 配制氯化铁溶液时需加入少量盐酸 | |
| B. | 金属钠保存在装有煤油的带玻璃塞的广口瓶中 | |
| C. | 保存液溴需用水封,放在带橡皮塞子的棕色细口瓶中 | |
| D. | 用稀硝酸洗去附在试管内壁的银镜 |
16.500℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
下列说法正确的是( )
| 反应时间min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 增大压强对正逆反应速率没有影响,平衡不移动 | |
| B. | 保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O(g),达到平衡时n(CO2)=0.40 mol | |
| C. | 保持其他条件不变,向平衡体系中再通入0.20mol H2O(g),与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | |
| D. | 由表格中数据得出,t1时刻该反应还未达到平衡 |
14.在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:
A(g)?2B(g)+C(g)+D(s)△H=+85.1kJ•mol-1
容器内气体总压强(P)与起始压强P0的比值随反应时间(t)数据见下表:
回答下列问题:
(1)下列操作能提高A转化率的是AD
A.升高温度 B.体系中通入A气体
C.通入稀有气体He,使体系压强增大到原来的5倍
D.若体系中的C为HCl,其它物质均难溶于水,滴入少许水
(2)该反应的平衡常数的表达式K=$\frac{{c}^{2}(B)×c(C)}{c(A)}$,前2小时C的反应速率是0.02 mol•L-1•h-1
(3)平衡时A的转化率为70%.
A(g)?2B(g)+C(g)+D(s)△H=+85.1kJ•mol-1
容器内气体总压强(P)与起始压强P0的比值随反应时间(t)数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| $\frac{P}{{P}_{0}}$ | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
(1)下列操作能提高A转化率的是AD
A.升高温度 B.体系中通入A气体
C.通入稀有气体He,使体系压强增大到原来的5倍
D.若体系中的C为HCl,其它物质均难溶于水,滴入少许水
(2)该反应的平衡常数的表达式K=$\frac{{c}^{2}(B)×c(C)}{c(A)}$,前2小时C的反应速率是0.02 mol•L-1•h-1
(3)平衡时A的转化率为70%.


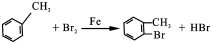 ,F的结构简式
,F的结构简式 .
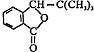
.
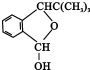 .
.