题目内容
4.某元素原子的价电子构型为4s24p1,它属于第四周期ⅢA族,属p区元素.分析 根据核外电子排布确定原子结构特点,可确定元素在周期表中的位置;ⅠA、ⅡA族最后填充s电子,为s区;ⅢA~零族为p区,第ⅢB~ⅤⅡB族和第ⅤⅢ为d区;ⅠB和ⅡB族为ds区,据此进行解答.
解答 解:某元素的原子的价电子构型为4s24p1,它在周期表中的位置是第4周期ⅢA族,为Ga;
根据ⅢA~零族为p区可知,该元素最后填充的为p电子,故属于p区元素,
故答案为:四;ⅢA;p.
点评 本题考查原子核外电子的排布,题目难度中等,明确原子结构与元素周期表的关系为解答关键,注意掌握原子核外电子的排布规律,试题培养了学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.化学实验操作中必须十分重视安全问题.下列处理方法不正确的是( )
| A. | 不慎打翻燃着的酒精灯,立即用湿抹布盖灭 | |
| B. | 浓碱液滴在皮肤上,立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 给盛有液体的试管加热时,要不断移动试管或加入碎瓷片 | |
| D. | 金属钠着火时,立即用泡沫灭火器进行灭火 |
12.化学反应中,在一定条件(如加热)下有时仍存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况.下列反应中属于这种情况的是( )
①过量的Zn与浓硫酸溶液反应
②过量的二氧化锰与浓盐酸反应
③过量的铜与浓硫酸反应
④过量的铜与稀硝酸反应
⑤常温下过量浓硫酸与铝反应.
①过量的Zn与浓硫酸溶液反应
②过量的二氧化锰与浓盐酸反应
③过量的铜与浓硫酸反应
④过量的铜与稀硝酸反应
⑤常温下过量浓硫酸与铝反应.
| A. | ②③⑤ | B. | ②③④ | C. | ①④⑤ | D. | ①②③④⑤ |
19.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是几种短周期元素的原子半径及主要化合价:
(1)用元素符号标出A、C、D、F在元素周期表中的相应位置(以下为元素周期表的一部分).
(2)A元素处于周期表中三周期IIA族.
(3)写出D离子的结构示意图 .
.
(4)上述A~F六种元素最高价氧化物对应水化物中酸性最强的是HClO4(填化学式).
(5)C元素气态氢化物的电子式为 .它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
.它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
(6)B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(7)元素E与元素F对比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是CD(填选项字母).
A.气态氢化物水溶液的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.气态氢化物的稳定性.
| 元素(或元 素代码) | 铍 | A | B | C | D | E | F |
| 原子半径 (10-10m) | 0.89 | 1.60 | 1.43 | 0.75 | 0.74 | 1.02 | 0.99 |
| 最高价态 | +2 | +2 | +3 | +5 | - | +6 | +7 |
| 最低价态 | - | - | - | -3 | -2 | -2 | -1 |
(2)A元素处于周期表中三周期IIA族.
(3)写出D离子的结构示意图
 .
.(4)上述A~F六种元素最高价氧化物对应水化物中酸性最强的是HClO4(填化学式).
(5)C元素气态氢化物的电子式为
 .它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
.它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.(6)B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(7)元素E与元素F对比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是CD(填选项字母).
A.气态氢化物水溶液的酸性 B.气态氢化物的沸点
C.单质与氢气反应的难易程度 D.气态氢化物的稳定性.
9.下列事实中,可以证明Al2O3中一定存在离子键的是( )
| A. | 易溶于水 | B. | 有较高的熔点 | C. | 熔化时能导电 | D. | 水溶液能导电 |
16.如表各组物质中,物质之间不可能实现如图所示转化的是( )
X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z
X$\stackrel{M}{→}$Y$\stackrel{M}{→}$Z
| 选项 | X | Y | Z | M |
| A | H2S | S | SO3 | O2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |
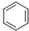 +CH3CH2CH2Cl$\stackrel{催化剂}{→}$
+CH3CH2CH2Cl$\stackrel{催化剂}{→}$ 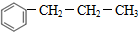 +HCl
+HCl
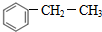 ,F的结构简式为
,F的结构简式为 ,
, .
.