题目内容
16.银锌碱性电池的电解质溶液为KOH溶液,电池放电时发生的总反应为Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag,下列说法不正确的是( )| A. | 放电时OH-向负极移动 | |
| B. | Ag2O2在反应中既是氧化剂又是还原剂 | |
| C. | 每生成1mol Ag外电路转移2 mol电子 | |
| D. | 负极反应为:Zn+4OH--2e-═Zn(OH)42- |
分析 根据Ag2O2+2Zn+4KOH+2H2O=2K2Zn(OH)4+2Ag可知,Ag2O2在反应中Ag和O元素的化合价降低,被还原,应为原电池正极,电极反应式为Ag2O2+2H2O+4e-=2Ag+4OH-,Zn元素化合价升高,被氧化,应为原电池负极,电极反应式为Zn+4OH--2e-═Zn(OH)42-,以此解答该题.
解答 解:A.放电时阴离子向原电池负极移动,阳离子向原电池正极移动,所以OH-向负极移动,故A正确;
B.Ag2O2在反应中Ag和O元素的化合价降低,被还原,Ag2O2在反应中为氧化剂,故B错误;
C.负极反应式为Ag2O2+2H2O+4e-=2Ag+4OH-,每生成1molAg外电路转移2mol电子,故C正确;
D.Zn元素化合价升高,被氧化,应为原电池负极,电极反应式为Zn+4OH--2e-═Zn(OH)42-,故D正确.
故选B.
点评 本题考查原电池知识,题目难度中等,注意电极反应式的书写,为解答该题的关键,易错点为Ag2O2在反应中Ag和O元素的化合价的变化.

练习册系列答案
相关题目
6.食品香精“菠萝酯”的生产路线(反应条件略去)如下.下列叙述不正确的是( )
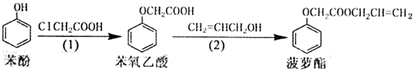
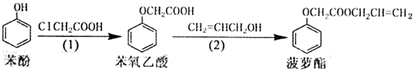
| A. | 苯氧乙酸的分子式为C8H8O3 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| D. | 步骤(2)产物中残留的烯丙醇可用溴水检验 |
7.某元素X的气态氢化物的分子式为H2X,则X的最高正价含氧酸的分子式为( )
| A. | H2S | B. | HNO3 | C. | H2SO4 | D. | H2SO3 |
4.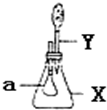 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
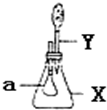 如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y不可能是( )
如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起.气体X和液体Y不可能是( )| A. | X是HCl,Y是蒸馏水 | B. | X是CO2,Y是稀H2SO4 | ||
| C. | X是SO2,Y是NaOH溶液 | D. | X是NH3,Y是NaNO3溶液 |
11.在密闭容器中盛有H2、O2、Cl2的混合气体,用电火花使三种气体恰好完全反应,冷至室温得液态产物,溶质的质量分数为25.3%,则容器内原有H2、O2、Cl2的体积比为( )
| A. | 6:3:1 | B. | 9:6:1 | C. | 13:6:1 | D. | 26:192:71 |
1.硫酸镁和硫酸铝的混合溶液中,Al3+ 离子的浓度为0.2mol•L-1,SO42- 离子的浓度为0.4mol•L-1,则混合溶液中Mg2+离子物质的量的浓度为( )
| A. | 0.4mol•L-1 | B. | 0.3mol•L-1 | C. | 0.2mol•L-1 | D. | 0.1mol•L-1 |
8.某实验室用下列溶质配制一种混合溶液,已知溶液中:c(K+)=c(Cl-)=$\frac{1}{3}$ c(Na+)=$\frac{2}{3}$c(SO42-),则其溶质可能是( )
| A. | MgCl2、Na2SO4、K2SO4 | B. | KCl、Na2SO4、NaCl | ||
| C. | NaCl、Na2SO4、K2SO4 | D. | KCl、Na2SO4、K2SO4 |
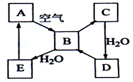 如图表示某固态单质A(淡黄色)及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A(淡黄色)及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.