题目内容
将含1mol Na和1mol Al的合金加入足量的水中,下列描述不正确的是( )
| A、金属Al无剩余 |
| B、c(Na+)=c(AlO-2) |
| C、生成气体为2mol |
| D、c(Na+)=c(Al3+) |
考点:钠的化学性质,镁、铝的重要化合物
专题:计算题,元素及其化合物
分析:等物质的量的Na和Al两种金属加入足量的水中,发生的化学反应有:2Na+2H2O=2NaOH+H2 ↑①,2NaOH+2Al+2H2O=2NaAlO2+3H2↑②,将方程式①+②得:2Na+4H2O+2Al=2NaAlO2+4H2 ↑,根据钠和铝之间的关系式分析判断.
解答:
解:等物质的量的Na和Al两种金属加入足量的水中,发生的化学反应有:2Na+2H2O=2NaOH+H2 ↑①,2NaOH+2Al+2H2O=2NaAlO2+3H2↑②,将方程式①+②得:2Na+4H2O+2Al=2NaAlO2+4H2 ↑,
A.根据方程式知,当钠和铝的物质的量相等时,恰好反应生成偏铝酸钠和氢气,金属没有剩余,故A正确;
B.偏铝酸根离子是弱离子能发生水解反应,所以钠离子的浓度大于偏铝酸根离子的浓度,故B错误;
C.由2Na+4H2O+2Al=2NaAlO2+4H2 ↑,可知生成氢气为1mol×
=2mol,故C正确;
D.最终溶液为偏铝酸钠,不存在Al3+离子,故D错误,
故选BD.
A.根据方程式知,当钠和铝的物质的量相等时,恰好反应生成偏铝酸钠和氢气,金属没有剩余,故A正确;
B.偏铝酸根离子是弱离子能发生水解反应,所以钠离子的浓度大于偏铝酸根离子的浓度,故B错误;
C.由2Na+4H2O+2Al=2NaAlO2+4H2 ↑,可知生成氢气为1mol×
| 4 |
| 2 |
D.最终溶液为偏铝酸钠,不存在Al3+离子,故D错误,
故选BD.
点评:本题考查了钠和铝的化学性质,难度不大,B选项是易错点,学生容易忽略盐类水解.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
下列物质中,属于强电解质的是( )
| A、Cu |
| B、H2O |
| C、H2SO4 |
| D、CH3COOH |
下列化学用语,应用正确的是( )
A、硝基苯的结构简式是: |
B、乙炔的电子式是: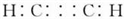 |
C、乙醚分子的球棍模型是: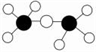 |
| D、甲酸中存在-CHO和-COOH两种官能团 |
下列反应中,属于加成反应的是( )
| A、甲烷与氯气混合,光照一段时间后黄绿色消失 |
| B、乙烯使酸性高锰酸钾溶液褪色 |
| C、将苯滴入少量到溴水中,振荡后水层接近无色 |
| D、乙烯使溴水褪色 |
现有C6H6 和C6H6O组成的混合物中,碳的质量分数为a%,则氧的质量分数为( )
A、(1-a%)×
| ||
B、a%×
| ||
| C、1-a% | ||
| D、(1-13a%/12) |
含H原子个数为1.806x1023个NH3,其质量为( )
| A、17克 | B、0.17克 |
| C、1.7克 | D、5.4克 |
实验室用锌片与2mol/L硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
| A、加入硫酸钾溶液 |
| B、加入几滴硫酸铜溶液 |
| C、改用热的2mol/L硫酸溶液 |
| D、改用浓硫酸溶液 |
把金属钠投入下列溶液中,有气体产生且溶液质量增加的是( )
| A、FeCl3溶液 |
| B、C2H5OH |
| C、饱和NaOH溶液 |
| D、CuSO4溶液 |