题目内容
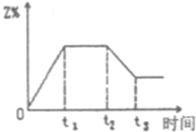 一定条件下,向某密闭容器中加入2molX发生如下反应:2X(g)?2Y(g)+Z(g)△H<0,在t1时刻达到平衡,然后在t2时刻改变某条件,到t3时刻又建立平衡,Z的百分含量变化如图所示,则t2时刻改变的条件是( )
一定条件下,向某密闭容器中加入2molX发生如下反应:2X(g)?2Y(g)+Z(g)△H<0,在t1时刻达到平衡,然后在t2时刻改变某条件,到t3时刻又建立平衡,Z的百分含量变化如图所示,则t2时刻改变的条件是( )| A、升高温度 | B、减小压强 | C、恒压条件下加入2molX | D、加入催化剂 |
分析:根据图象知,在t2时刻改变某条件,到t3时刻又建立平衡,Z的百分含量减少,说明该反应向逆反应方向移动,根据外界条件对化学平衡的影响分析判断.
解答:解:由2X(g)?2Y(g)+Z(g)△H<0知,该反应是一个反应前后气体体积减小、正反应方向是放热的化学反应.
A、该反应正反应是放热反应,升高温度导致化学平衡向逆反应方向移动,Z的百分含量降低,所以A符合图象,故A正确.
B、该反应正反应是气体体积减小的化学反应,减小压强,平衡向正反应方向移动导致Z的百分含量增大,所以B不符合图象,故B错误.
C、恒压条件下加入2molX导致容器的体积增大,对于原平衡体系来说相当于减小压强,平衡向正反应方向移动导致Z的百分含量增大,所以C不符合图象,故C错误.
D、加入催化剂化学平衡不移动,所以Z的百分含量不变,与图象不符合,故D错误.
故选A.
A、该反应正反应是放热反应,升高温度导致化学平衡向逆反应方向移动,Z的百分含量降低,所以A符合图象,故A正确.
B、该反应正反应是气体体积减小的化学反应,减小压强,平衡向正反应方向移动导致Z的百分含量增大,所以B不符合图象,故B错误.
C、恒压条件下加入2molX导致容器的体积增大,对于原平衡体系来说相当于减小压强,平衡向正反应方向移动导致Z的百分含量增大,所以C不符合图象,故C错误.
D、加入催化剂化学平衡不移动,所以Z的百分含量不变,与图象不符合,故D错误.
故选A.
点评:本题以图象为载体考查了外界条件对化学平衡的影响,在分析图象题时要注意纵横坐标的含义、曲线的变化趋势、拐点等,根据图象联系规律,根据规律分析解答从而作出正确判断.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
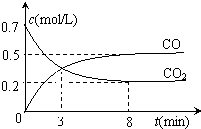 一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0.反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,下列说法不正确的是( )
一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0.反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,下列说法不正确的是( )A、该反应的平衡常数表达式为K=
| ||
B、升高温度后达新平衡时,
| ||
| C、3分钟时,CO和CO2的浓度相等,反应达到平衡状态 | ||
| D、8分钟内CO的平均反应速率v(CO)=0.0625 mol?L-1?min-1 |
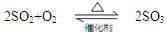 的说法不正确的是
的说法不正确的是