题目内容
6.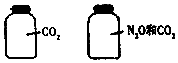 如图所示.两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不反应)关系一定不正确的是( )
如图所示.两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不反应)关系一定不正确的是( )| A. | 所含氧原子数相等 | B. | 气体的总质量相等 | ||
| C. | 气体的平均摩尔质量相等 | D. | 气体的密度相等 |
分析 同温同压下,体积之比等于物质的量之比,两瓶气体的物质的量相等,N2O和CO2的摩尔质量都是44g/mol,则两个集气瓶中气体质量相等;N2O和CO2含有的O原子数目不同,则两个集气瓶中含有O原子数不同,依据ρ=$\frac{m}{V}$判断密度大小,据此进行解答.
解答 解:同温同压下,体积之比等于物质的量之比,两瓶气体的物质的量相等,
A.N2O和CO2含有的O原子数目不同,所以虽然两瓶中气体物质的量相等,但是二者所含氧原子数不同,故A选;
B.N2O和CO2的摩尔质量都是44g/mol,两瓶气体物质的量相等,则二者气体的总质量相等,故B不选;
C.N2O和CO2的摩尔质量都是44g/mol,混合气体的平均摩尔质量为44g/mol,故C不选;
D.两瓶气体的体积相等,质量相等,则依据ρ=$\frac{m}{V}$可知,二者气体的密度相等,故D不选;
故选:A.
点评 本题考查阿伏伽德罗定律及其推论,熟练掌握公式中各个物理量的关系是解本题关键,注意气体摩尔体积适用范围及适用条件,题目难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
17.下面关于石油加工的过程是物理变化的是( )
| A. | 裂化 | B. | 裂解 | C. | 重整 | D. | 石油的分馏 |
14.用NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 相同质量的铝,分别与足量的盐酸和氢氧化钠溶液反应放出的氢气体积一定不相同 | |
| B. | 56gFe与足量盐酸反应转移电子数为3NA | |
| C. | 任何条件下,22.4LNH3与18gH2O所含电子数均为10NA | |
| D. | 46gNO2和N2O4的混合物含有的原子数为3NA |
11.四种仪器中,不能用来加热的是( )
| A. |  烧杯 | B. |  容量瓶 | C. |  试管 | D. |  烧瓶 |
18.下列有关叙述正确的是( )
| A. | 在NaHS溶液中滴人少量CuCl2溶液,产生黑色沉淀,HS-水解程度增大,pH增大 | |
| B. | 常温下,由于HCO3-水解显碱性,所以饱和NaHCO3溶液显碱性 | |
| C. | 泡沫灭火器是利用Al2(SO4)3溶液与饱和NaHCO3溶液混合产生气体 | |
| D. | 配制氯化铝溶液时,先将氯化铝溶于浓硫酸,再加水稀释 |
2.下列说法不正确的是( )
| A. | 铜呈紫红色.可与氯化铁溶液反应制作印刷电路板 | |
| B. | 可用丁达尔效应区分胶体和溶液 | |
| C. | 工业上用焦炭在高温下还原二氧化硅可直接得到高纯度的硅 | |
| D. | 镁合金大量用于制造火箭、导弹和飞机的部件 |