题目内容
(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放出256kJ的热量.
①写出该反应的热化学方程式 .
②又已知H2O(l)=H2O(g),△H=44kJ?mol-1,则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ.
(2)实验室用足量的金属锌与体积、浓度一定的稀硫酸反应制取氢气时(不考虑温度变化),要想使反应速率减慢,又不影响产生氢气的总量,下列措施中能达到目的是 .
①加入少量固体碳酸钠; ②加入少量固体醋酸钠;
③加入适量的硫酸钠溶液; ④加入适量的硝酸钠溶液;
⑤滴加少量CuSO4溶液; ⑥加热.
①写出该反应的热化学方程式
②又已知H2O(l)=H2O(g),△H=44kJ?mol-1,则16g液态肼与液态双氧水反应生成液态水时放出的热量是
(2)实验室用足量的金属锌与体积、浓度一定的稀硫酸反应制取氢气时(不考虑温度变化),要想使反应速率减慢,又不影响产生氢气的总量,下列措施中能达到目的是
①加入少量固体碳酸钠; ②加入少量固体醋酸钠;
③加入适量的硫酸钠溶液; ④加入适量的硝酸钠溶液;
⑤滴加少量CuSO4溶液; ⑥加热.
考点:热化学方程式,化学反应速率的影响因素
专题:化学反应中的能量变化,化学反应速率专题
分析:(1)①反应方程式为:N2H4+2H2O2=N2+4H2O,根据0.4mol液态肼放出的热量,计算1mol液态肼放出的热量,进而写出热化学方程式;
②结合上述写出的热化学方程式和谁转化的热化学方程式,根据盖斯定律合并写出生成液态水时的热化学方程式进行计算;
(2)要使氢气的生成速率减慢,但又不影响其总量,则减小氢离子浓度,而不能减小氢离子的物质的量,以此来解答.
②结合上述写出的热化学方程式和谁转化的热化学方程式,根据盖斯定律合并写出生成液态水时的热化学方程式进行计算;
(2)要使氢气的生成速率减慢,但又不影响其总量,则减小氢离子浓度,而不能减小氢离子的物质的量,以此来解答.
解答:
解:(1)①反应方程式为:N2H4+2H2O2═N2+4H2O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为
kJ=640kJ,
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-640kJ/mol,
故答案为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-640 kJ?mol-1;
②a、N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63KJ/mol;
b、H2O(g)=H2O(l)△H=-44KJ/mol;
依据盖斯定律a+b×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l)△H=-817KJ/mol;化学方程式中32g全部反应放热817KJ,16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是408kJ,
故答案为:408;
(2)①加入少量固体碳酸钠,会和硫酸之间反应,产生二氧化碳,能使使反应速率减慢,会影响产生氢气的总量,故错误;
②加入少量固体醋酸钠,会和硫酸之间反应生成醋酸,醋酸是弱酸,能使使反应速率减慢,不会影响产生氢气的总量,故正确;
③加入适量的硫酸钠溶液,减小氢离子浓度,而不能减小氢离子的物质的量,则反应速率减慢,不影响氢气的总量,故正确;
④加入适量的硝酸钠溶液,相当于溶液中含有硝酸,和金属反应不会产生氢气,所以会影响氢气的总量,故错误;
⑤滴加少量CuSO4溶液,会形成原电池,加快反应速率,故错误;
⑥加热会加快反应速率,故错误;
故选②③.
| 256 |
| 0.4 |
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-640kJ/mol,
故答案为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-640 kJ?mol-1;
②a、N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63KJ/mol;
b、H2O(g)=H2O(l)△H=-44KJ/mol;
依据盖斯定律a+b×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l)△H=-817KJ/mol;化学方程式中32g全部反应放热817KJ,16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是408kJ,
故答案为:408;
(2)①加入少量固体碳酸钠,会和硫酸之间反应,产生二氧化碳,能使使反应速率减慢,会影响产生氢气的总量,故错误;
②加入少量固体醋酸钠,会和硫酸之间反应生成醋酸,醋酸是弱酸,能使使反应速率减慢,不会影响产生氢气的总量,故正确;
③加入适量的硫酸钠溶液,减小氢离子浓度,而不能减小氢离子的物质的量,则反应速率减慢,不影响氢气的总量,故正确;
④加入适量的硝酸钠溶液,相当于溶液中含有硝酸,和金属反应不会产生氢气,所以会影响氢气的总量,故错误;
⑤滴加少量CuSO4溶液,会形成原电池,加快反应速率,故错误;
⑥加热会加快反应速率,故错误;
故选②③.
点评:本题考查热化学方程式的书写、化学反应速率的影响因素,为高频考点,把握氢离子浓度、物质的量的变化为解答的关键,注意发生的氧化还原反应是否生成氢气,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
下列实验操作或对实验事实的描述正确的是 ( )
| A、不宜用瓷坩埚灼烧氢氧化钠或碳酸钠 |
| B、定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容 |
| C、使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大 |
| D、用铝箔包住部分被氧化成Na2O的钠块,并用镊子夹住在水槽中反应,用倒置的量筒量取生成气体的体积,可以计算钠块中钠单质的质量分数 |
| E、用托盘天平称量11.74g氯化钠晶体 |
| F、为了使稀硫酸和锌制取氢气的速率加快,可向稀硫酸中加入用铜网包裹的锌粒 |
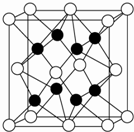 X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.回答下列问题(相关回答均用元素符号表示):
X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.回答下列问题(相关回答均用元素符号表示):
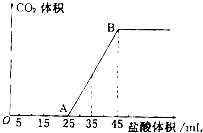 实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题
实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题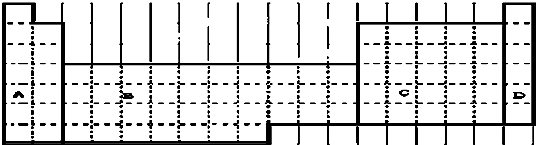
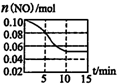 汽车尾气中含有NO和CO等有害气体.选择适当的催化剂可将CO、NO转化为无毒气体.
汽车尾气中含有NO和CO等有害气体.选择适当的催化剂可将CO、NO转化为无毒气体.