题目内容
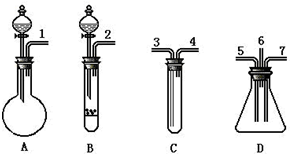 根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验.可选用的仪器如图所示:
根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验.可选用的仪器如图所示:可选用的试剂:①盐酸,②溴水,③Na2SO3固体,④FeS固体(难溶于水的块状固体,与酸反应制取硫化氢),⑤品红溶液,⑥氢氧化钠溶液.
试回答下列问题:
(1)用胶管连接上述仪器组合成整套装置,正确的连接顺序是(用数字1、2、…、表示)
(2)上述装置中,应加入的试剂( 从①--⑥中选取,填写序号,否则不得分)是A
(3)表现SO2氧化性的实验是上述仪器中的
(4)写出A和D中所发生的化学反应方程式:
(5)该实验装置存在明显缺陷,请作评价并加以改正.
考点:性质实验方案的设计,二氧化硫的化学性质
专题:氧族元素
分析:验证SO2既有氧化性又有还原性的实验,由图可知,A中发生①③物质的反应生成SO2,B中发生①④物质的反应生成H2S,在C中加溴水,1与3相连,溴水褪色,发生SO2+Br2+2H2O=H2SO4+2HBr;4与5相连,同时2与7相连,二氧化硫与硫化氢均进入D中发生2H2S+SO2=3S↓+2H2O,为防止污染环境,然后出气口6与3相连,此时C中为NaOH溶液进行尾气处理,以此来解答.
解答:
解:验证SO2既有氧化性又有还原性的实验,由图可知,A中发生①③物质的反应生成SO2,B中发生①④物质的反应生成H2S,在C中加溴水,1与3相连,溴水褪色,发生SO2+Br2+2H2O=H2SO4+2HBr;4与5相连,同时2与7相连,二氧化硫与硫化氢均进入D中发生2H2S+SO2=3S↓+2H2O,然后出气口6与3相连,此时C中为NaOH溶液进行尾气处理,
(1)由上述分析可知,上述仪器组合成整套装置,装置顺序为A、C、D(同时连B、D)、C,则正确的连接顺序是1→3→4→5(同时连2→7)→6,
故答案为:1→3→4→5(同时连2→7)→6;
(2)由上述分析可知,A中试剂为①③,B中试剂为①④,C中分别试剂为②或⑥,故答案为:①③;①④;②或⑥;
(3)D中发生2H2S+SO2=3S↓+2H2O,S元素的化合价降低,体现二氧化硫的氧化性,观察到装置内壁上有淡黄色的固体析出和液滴生成;C中发生SO2+Br2+2H2O=H2SO4+2HBr,S元素的化合价升高,体现二氧化硫的还原性,观察到溴水褪色,
故答案为:D;装置内壁上有淡黄色的固体析出和液滴生成;C;溴水褪色;
(4)A和D中所发生的化学反应方程式分别为Na2SO3+2HCl=2NaCl+H2O+SO2↑、2H2S+SO2=3S↓+2H2O,B和C中所发生的离子方程式分别为FeS+2H+=H2S↑+Fe2+、SO2+Br2+2H2O=SO42-+4H++2Br-,故答案为:Na2SO3+2HCl=2NaCl+H2O+SO2↑;2H2S+SO2=3S↓+2H2O;FeS+2H+=H2S↑+Fe2+;SO2+Br2+2H2O=SO42-+4H++2Br-;
(5)该实验中二氧化硫、硫化氢、溴蒸气均为有毒气体,严重污染大气,必须净化后再放空,则装置D的出气管应连接盛有NaOH溶液的C装置3口,
故答案为:装置D的出气管应连接盛有NaOH溶液的C装置3口.
(1)由上述分析可知,上述仪器组合成整套装置,装置顺序为A、C、D(同时连B、D)、C,则正确的连接顺序是1→3→4→5(同时连2→7)→6,
故答案为:1→3→4→5(同时连2→7)→6;
(2)由上述分析可知,A中试剂为①③,B中试剂为①④,C中分别试剂为②或⑥,故答案为:①③;①④;②或⑥;
(3)D中发生2H2S+SO2=3S↓+2H2O,S元素的化合价降低,体现二氧化硫的氧化性,观察到装置内壁上有淡黄色的固体析出和液滴生成;C中发生SO2+Br2+2H2O=H2SO4+2HBr,S元素的化合价升高,体现二氧化硫的还原性,观察到溴水褪色,
故答案为:D;装置内壁上有淡黄色的固体析出和液滴生成;C;溴水褪色;
(4)A和D中所发生的化学反应方程式分别为Na2SO3+2HCl=2NaCl+H2O+SO2↑、2H2S+SO2=3S↓+2H2O,B和C中所发生的离子方程式分别为FeS+2H+=H2S↑+Fe2+、SO2+Br2+2H2O=SO42-+4H++2Br-,故答案为:Na2SO3+2HCl=2NaCl+H2O+SO2↑;2H2S+SO2=3S↓+2H2O;FeS+2H+=H2S↑+Fe2+;SO2+Br2+2H2O=SO42-+4H++2Br-;
(5)该实验中二氧化硫、硫化氢、溴蒸气均为有毒气体,严重污染大气,必须净化后再放空,则装置D的出气管应连接盛有NaOH溶液的C装置3口,
故答案为:装置D的出气管应连接盛有NaOH溶液的C装置3口.
点评:本题考查性质实验方案的设计,为高频考点,把握还原性与氧化性的实验中发生的化学反应进行实验设计为解答的关键,注重氧化还原反应、实验技能、化学与环境的综合考查,题目难度中等.

练习册系列答案
相关题目
下列关于容量瓶及其使用方法的叙述,正确的是( )
| A、是配制一定物质的量浓度的溶液的专用仪器 |
| B、容量瓶可以用来加热 |
| C、不能用容量瓶贮存配制好的溶液 |
| D、可以用500mL容量瓶配制250mL溶液 |
下列说法正确的是( )
| A、PM2.5作为空气质量预报的一项重要指标,它是指空气中直径大于或等于2.5μm的颗粒物,该值越高,代表空气污染程度越严重 |
| B、新型材料聚酯纤维、光导纤维都属于有机高分子 |
| C、上海世博会很多展馆采用光电转化装置,体现当今“低碳”经济的理念 |
| D、塑化剂是一种化工塑料软化剂,可以大量添加到婴幼儿玩具中 |
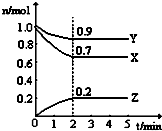 某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: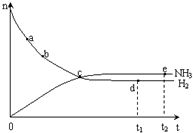 合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0
合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0