题目内容
6.下列化学反应的离子方程式,书写不正确的是( )| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 向氯化铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 氯化亚铁溶液中通入少量氯气:Cl2+2Fe2+═2Fe3++2Cl- | |
| D. | 往明矾溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++2SO42-+Al3++4OH-═2BaSO4↓+AlO2-+2H2O |
分析 A.2mol钠与水反应生成1mol氢气,该反应不满足电子守恒;
B.一水合氨为弱碱,离子方程式中一水合氨不能拆开,且反应生成氢氧化铝沉淀;
C.氯化亚铁与氯气反应生成氯化铁;
D.硫酸根离子恰好沉淀时,铝离子与氢氧根离子恰好反应生成偏铝酸根离子.
解答 解:A.钠与水反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.向氯化铝溶液中加入过量氨水,反应生成氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.氯化亚铁溶液中通入少量氯气,反应生成氯化铁,反应的离子方程式为:Cl2+2Fe2+═2Fe3++2Cl-,故C正确;
D.往明矾溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全,反应的离子方程式为:2Ba2++2SO42-+Al3++4OH-═2BaSO4↓+AlO2-+2H2O,故D正确;
故选AB.
点评 本题考查了离子方程式的判断,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
17.下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入CO2至过量
②向Fe(OH)3胶体中逐滴加入稀盐酸至过量
③向NaAlO2 溶液中通入CO2至过量
④向 AlCl3溶液中加入 Ba(OH)2溶液至过量
⑤向CaCl2溶液中通入 CO2 至过量.
①向饱和碳酸钠溶液中通入CO2至过量
②向Fe(OH)3胶体中逐滴加入稀盐酸至过量
③向NaAlO2 溶液中通入CO2至过量
④向 AlCl3溶液中加入 Ba(OH)2溶液至过量
⑤向CaCl2溶液中通入 CO2 至过量.
| A. | ①③⑤ | B. | ①② | C. | ①③ | D. | ②③⑤ |
14.为了检验SO2的性质,下列实验现象、解释与结论均正确的是( )
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 将SO2气体通入KMnO4(H+)溶液中 | 溶液褪色 | SO2有漂白性 |
| B | 将SO2气体通入H2S溶液中 | 溶液变浑浊 | SO2有氧化性 |
| C | 将SO2气体通入紫色石蕊溶液中 | 溶液先变红色后褪色 | SO2是酸性氧化物 |
| D | 将SO2气体通入Ca(ClO)2溶液中 | 溶液变浑浊 | 亚硫酸的酸性比次氯酸的酸性强 |
| A. | A | B. | B | C. | C | D. | D |
11.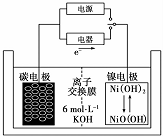 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为原电池的负极 | |
| D. | 放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O |
18.下列物质的水溶液因水解而呈碱性的是( )
| A. | NaOH | B. | NH4Cl | C. | NaCl | D. | Na2CO3 |
2.配制200mL 0.100mol•L-1盐酸溶液时,下列实验操作使所配的溶液浓度偏大的是( )
| A. | 用量筒量取所需的浓盐酸时仰视读数 | |
| B. | 用量筒量取的浓盐酸时,量筒里有少许蒸馏水 | |
| C. | 定容时,仰视标线 | |
| D. | 定容后倒转容量瓶数次摇匀,发现液面最低点低于标线,再补加几滴蒸馏水至标线 |
3.根据能量变化示意图,下列说法正确的是( )
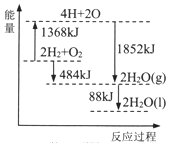

| A. | 拆开2molH2(g)和1 molO2(g)中的化学键,共放出1368 kJ能量 | |
| B. | 1 molH2和0.5molO2的能量之和比1 molH2O(1)的能量大242 kJ | |
| C. | 2H2O(g)=2H2(g)+O2(g)△H=+484KJ/mol | |
| D. | 2H2(g)+O2(g)=2H2O(1)△H=572KJ/mol |
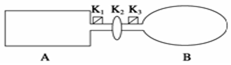 A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同.(已知:2NO2(g)?N2O4(g)△H<0)
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同.(已知:2NO2(g)?N2O4(g)△H<0)