题目内容
 某离子晶体的晶胞结构如图所示,则该离子晶体的化学式为( )
某离子晶体的晶胞结构如图所示,则该离子晶体的化学式为( )| A、AB12C8 |
| B、ABC3 |
| C、AB2C3 |
| D、AB3C |
考点:晶胞的计算
专题:化学键与晶体结构
分析:晶胞中位于立方体顶点的离子被8个晶胞共有,位于立方体中心的离子被一个晶胞占有,位于棱上的离子被4个晶胞共用,利用均摊法确定其化学式.
解答:
解:A离子位于体心,所以该晶胞中含有1个A离子,B离子个数=12×
=3,C离子个数=8×
=1,所以该晶胞中A、B、C离子个数之比是1:3:1,所以其化学式为AB3C,
故选D.
| 1 |
| 4 |
| 1 |
| 8 |
故选D.
点评:本题考查了晶胞的计算,明确位于顶点、棱上、面心、体心上的离子被几个晶胞占有是解本题关键,利用均摊法即可分析解答,难度不大.

练习册系列答案
相关题目
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、16 g CH4中含有4 nA个C-H键 |
| B、1 mol/L NaCl溶液含有nA个Na+ |
| C、1 mol Cu和足量稀硝酸反应产生nA个NO分子 |
| D、标准状况下,22.4 L 己烯中含有nA个己烯分子 |
下列物质类别、名称(或俗名)、化学式相符的是( )
| A、碱性氧化物,氧化亚铁,Fe2O3 |
| B、酸,硫酸,H2SO3 |
| C、碱,熟石灰,CaO |
| D、酸性氧化物,干冰,CO2 |
下列各组物质的熔沸点按由低到高的顺序排列正确的是( )
| A、冰、干冰、氯化钠、金刚石 |
| B、汞、钠、烧碱、二氧化硅 |
| C、NaCl、KCl、CsCl |
| D、H2O、H2S、H2Se、H2Te |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、0.5 L 1 mol/L的Na2SO4溶液中,含有Na+的个数为NA |
| B、22.4 L N2含有氮原子的个数为2NA |
| C、1 mol钠与水反应生成氢气的分子数为0.5NA |
| D、NA个Cl2分子与水反应,转移的电子数为2NA |
温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤NaHCO3、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是( )
| A、③①④②⑥⑤ |
| B、①③⑥④②⑤ |
| C、③②①⑥④⑤ |
| D、⑤⑥②④①③ |
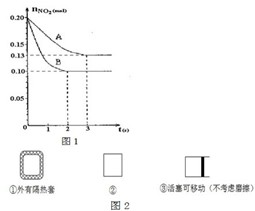 在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.
在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图1所示.