题目内容
化学方程式可简明地体现元素及其化合物的性质.已知:
氧化还原反应:
FeCl3+H2S=FeCl2+S;PbO2+4HCl=PbCl2+Cl2↑+2H2O
2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl;Cl2+2KOH=KCl+KClO+H2O
水溶液中的复分解反应:(Se元素的原子序数为34)
CuSO4+H2S=CuS↓+H2SO4;H2SeO4+2NaN3=Na2SeO4+2HN3;HN3+Na2S=NaN3+H2S
热分解反应:BaCO3
BaO+CO2↑;MgCO3
MgO+CO2↑;CuCO3
CuO+CO2↑
下列说法不正确的是( )
氧化还原反应:
FeCl3+H2S=FeCl2+S;PbO2+4HCl=PbCl2+Cl2↑+2H2O
2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl;Cl2+2KOH=KCl+KClO+H2O
水溶液中的复分解反应:(Se元素的原子序数为34)
CuSO4+H2S=CuS↓+H2SO4;H2SeO4+2NaN3=Na2SeO4+2HN3;HN3+Na2S=NaN3+H2S
热分解反应:BaCO3
| ||
| ||
| ||
下列说法不正确的是( )
| A、氧化性(酸性溶液):PbO2>Fe3+>S |
| B、还原性(碱性溶液):Fe(OH)2>KCl>Cl2 |
| C、酸性(水溶液):H2S>H2SO4>H2SeO4>HN3 |
| D、热稳定性:BaCO3>MgCO3>CuCO3 |
考点:氧化性、还原性强弱的比较,非金属在元素周期表中的位置及其性质递变的规律
专题:氧化还原反应专题
分析:A、根据氧化剂的氧化性大于氧化产物的氧化性判断;
B、根据还原剂的还原性大于还原产物的还原性来判断,在反应物中作还原剂的是该反应中所有物质中还原性最强的;
C、根据化学反应遵循强酸制弱酸的规律来判断;
D、分解温度越高,该物质越稳定.
B、根据还原剂的还原性大于还原产物的还原性来判断,在反应物中作还原剂的是该反应中所有物质中还原性最强的;
C、根据化学反应遵循强酸制弱酸的规律来判断;
D、分解温度越高,该物质越稳定.
解答:
解:A、在FeCl3+H2S=FeCl2+S反应中,氧化性:FeCl3>S,
在PbO2+4HCl=PbCl2+Cl2↑+2H2O,氧化性:PbO2>Cl2,
在2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl反应中,氧化性:Cl2>Fe3+,
则有:PbO2>Fe3+>S,故A正确;
B、在 2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl中,还原性:Fe(OH)2>KCl;
在 Cl2+2KOH=KCl+KClO+H2O反应中,Cl2既是氧化剂又是还原剂,其还原性介于高低价态产物之间KCl>Cl2>KClO;
故还原性应为:Fe(OH)2>KCl>Cl2,故B正确;
C、化学反应遵循强酸制弱酸的规律,在反应H2SeO4+2NaN3=Na2SeO4+2HN3中,酸性:H2SeO4>HN3,在反应中HN3+Na2S=NaN3+H2S,酸性:HN3>H2S,在CuSO4+H2S=CuS↓+H2SO4中,H2S为弱酸,H2SO4为强酸,CuS不溶于硫酸,该反应不符合强酸制弱酸的规律,但是满足复分解反应的条件所以能发生,
则酸性为:H2SO4>H2SeO4>HN3>H2S,故C错误;
D、分解温度越高,该物质越稳定,所以碳酸盐的稳定性大小顺序是BaCO3>MgCO3>CuCO3,故D正确.
故选C.
在PbO2+4HCl=PbCl2+Cl2↑+2H2O,氧化性:PbO2>Cl2,
在2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl反应中,氧化性:Cl2>Fe3+,
则有:PbO2>Fe3+>S,故A正确;
B、在 2Fe(OH)2+Cl2+2KOH=2Fe(OH)3+2KCl中,还原性:Fe(OH)2>KCl;
在 Cl2+2KOH=KCl+KClO+H2O反应中,Cl2既是氧化剂又是还原剂,其还原性介于高低价态产物之间KCl>Cl2>KClO;
故还原性应为:Fe(OH)2>KCl>Cl2,故B正确;
C、化学反应遵循强酸制弱酸的规律,在反应H2SeO4+2NaN3=Na2SeO4+2HN3中,酸性:H2SeO4>HN3,在反应中HN3+Na2S=NaN3+H2S,酸性:HN3>H2S,在CuSO4+H2S=CuS↓+H2SO4中,H2S为弱酸,H2SO4为强酸,CuS不溶于硫酸,该反应不符合强酸制弱酸的规律,但是满足复分解反应的条件所以能发生,
则酸性为:H2SO4>H2SeO4>HN3>H2S,故C错误;
D、分解温度越高,该物质越稳定,所以碳酸盐的稳定性大小顺序是BaCO3>MgCO3>CuCO3,故D正确.
故选C.
点评:本题考查氧化性、还原性、稳定性和酸性的比较,做题时注意积累比较物质的性质的规律和方法,题目难度中等,侧重于氧化还原反应知识的综合应用的考查.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列关于物质分类的说法正确的是( )
| A、漂白粉、胆矾都属于混合物 |
| B、氧化铝、氯化钠都属于离子化合物 |
| C、氯化铵、次氯酸都属于强电解质 |
| D、二氧化硫、二氧化氮都属于酸性氧化物 |
常温下,浓度均为0.1mol/L CH3COOH溶液和HCN溶液的pH分别为m和n(1<m<n).下列叙述中不正确的是( )
| A、常温下,pH相同的CH3COOH溶液和HCN溶液分别加水稀释相同的倍数时,前者pH变化小 |
| B、等温下,等浓度的CH3COONa和NaCN溶液pH,后者大 |
| C、HCN溶液和NaOH溶液不等体积混合后一定存在C(H+)-C(OH-)=C(CN-)-C(Na+) |
| D、溶液中由水电离出的c(H+),前者是后者的10m-n倍 |


 (5)下列关于化合物I、II、V、VI的说法正确的有
(5)下列关于化合物I、II、V、VI的说法正确的有
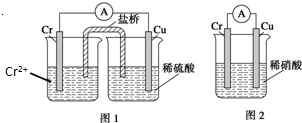 金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).
金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).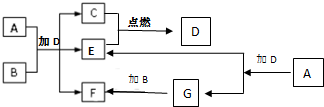 下列框图中各物质均为中学常见物质.A是淡黄色固体化合物,B、C、E为单质,其中C、E为气体,B为金属.常温、常压下D为无色液体.
下列框图中各物质均为中学常见物质.A是淡黄色固体化合物,B、C、E为单质,其中C、E为气体,B为金属.常温、常压下D为无色液体.