题目内容
7.(1)维生素C是一种水溶性的维生素,缺乏VC会使人患上坏血病.切取一片新鲜水果,向切面上滴加淀粉溶液和碘水,若出现褪色,说明新鲜水果中含有VC,这是利用VC具有还原(填“氧化”或“还原”)性质.(2)经科学测定,人体平均含氧65%,含碳18%,含氢10%(以上均为质量分数),则三种元素中原子数目最多的是H(填元素符号).
分析 (1)根据实验现象,确定维生素C的性质,缺少维生素C会患坏血病;
(2)设人体的质量为m,则人体中该元素原子的物质的量=m×$\frac{质量分数}{该元素的摩尔质量}$.
解答 解:(1)向一片新鲜水果的切面上滴加淀粉溶液和碘水,出现蓝色后又慢慢褪去,说明维生素C把单质碘还原为碘离子,故维生素C具有还原性,缺少维生素C医患坏血病,故答案为:坏血;褪色;还原;
(2)设人体的质量为m,则人体中该元素原子的物质的量=m×$\frac{质量分数}{该元素的摩尔质量}$,所以
n(C)=m×$\frac{18%}{12}$=0.012mmol,n(H)=m×$\frac{10%}{1}$=0.1mmol,n(O)=m×$\frac{65%}{16}$=0.041mmol
故答案为:H.
点评 本题考查了化学与生活,涉及维生素、物质的量的有关计算,题目难度不大,但易错,注意把握物质的量与质量有关计算公式的运用.

练习册系列答案
相关题目
1.A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中离子半径最小的,则它们的原子序数由小到大的顺序是( )
| A. | E、C、D、B、A | B. | B、A、E、D、C | C. | E、B、A、D、C | D. | A、B、C、D、E |
15.向含SO32-、Fe2+、Br-、I-各0.1mol的混合溶液中通入Cl2,Cl2与它们可能发生如下四个反应:①SO32-+Cl2+H2=SO42-+2Cl-+2H+,②2Fe2++Cl2=2Fe3++2Cl-,③2Br-+Cl2=Br2+2Cl-,④2I-+Cl2=I2+2Cl-.当通入0.2molCl2时,发生的反应是( )
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
12.以下物质;(1)甲烷;(2)苯;(3)聚乙烯;(4)苯乙烯;(5)2-丁炔;(6)环己烷;(7)邻二甲苯.既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
| A. | (1)(2)(3)(4)(5) | B. | (4)(5)(7)) | C. | (4)(5) | D. | (3)(4)(5)(7) |
17.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
| A. | 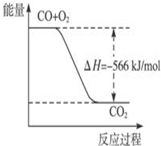 图可表示由CO生成CO2的反应过程和能量关系 | |
| B. | CO的燃烧热为566 kJ/mol | |
| C. | Na2O2(s)+CO2(s)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226 kJ/mol | |
| D. | CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023 |

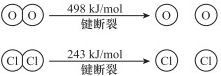
 .
.