题目内容
12.根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确的是( )①ClO3-+5Cl-+6H+═3Cl2+3H2O
②2FeCl3+2KI═2FeCl2+2KCl+I2
③2FeCl2+Cl2═2FeCl3.
| A. | ClO3->Cl2>I2>Fe3+ | B. | Cl2>ClO3->I2>Fe3+ | ||
| C. | ClO3->Cl2>Fe3+>I2 | D. | ClO3->Fe3+>Cl2>I2 |
分析 氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此分析.
解答 解:①中ClO3-是氧化剂,Cl2是氧化产物,所以氧化性ClO3->Cl2,
②中Fe3+是氧化剂,I2是氧化产物,所以氧化性:Fe3+>I2,
③中Cl2是氧化剂,Fe3+是氧化产物,所以氧化性:Cl2>Fe3+,
综上得氧化性顺序为ClO3->Cl2>Fe3+>I2.
故选C.
点评 本题考查氧化性强弱的判断规律:氧化剂的氧化性强于氧化产物的氧化性,可以根据所学知识进行回答,难度不大,关键正确判断氧化剂、还原剂.

练习册系列答案
相关题目
20.下列反应的离子方程式正确的是( )
| A. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O═2OH-+H2↑+Cl2↑ | |
| B. | 向偏铝酸钠溶液中通入过量的CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 向NH4HCO3稀溶液中滴加过量Ca(OH)2溶液:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O | |
| D. | 向CuSO4溶液中滴加过量氨水:Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+ |
7.下列有关溶液中离子存在和转化的表达合理的是( )
| A. | 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-═A2-+H2O | |
| B. | 标准状况下,将1.12LCO2气体通入1L0.1mol/L的NaAlO2溶液中:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 由水电离出的c(H+)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| D. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓ |
17.下列物质中,分子内和分子间均可形成氢键的是( )
| A. | NH3 | B. | B | C. | H2O | D. | C2H5OH |
4.水晶是重要的首饰用品,其主要成分是SiO2,下列有关SiO2的说法正确的是( )
| A. | 水晶能溶于水生成H2SiO3 | |
| B. | SiO2是酸性氧化物,不能与任何酸反应 | |
| C. | SiO2既能溶于NaOH溶液,又能溶于HF,因此属于两性氧化物 | |
| D. | SiO2对应的H2SiO3是一种弱酸,酸性比碳酸还弱 |
1.下列有关非金属元素说法正确的是( )
| A. | 二氧化氯具有还原性,可用于自来水的杀菌消毒 | |
| B. | SO2具有氧化性,可用于漂白纸浆 | |
| C. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| D. | 硅是重要的半导体材料,常用于制作光导纤维 |
2.下列关于著名科学家及其成就的描叙不正确的是( )
| A. | 德国化学家维勒第一次人工合成了尿素,从而揭开了人工合成有机物的序幕 | |
| B. | 中国化学家侯德榜成功发明了侯氏制碱法,打破了外国当时对中国的相关技术封锁 | |
| C. | 英国科学家卢瑟福根据α粒子散射实验提出了“葡萄干面包式”原子结构模型 | |
| D. | 俄国化学家门捷列夫在前人基础上研究提出了元素周期律并列出了第一张元素周期表 |
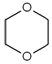 ).
).