题目内容
对于如图,下列说法正确的是( )
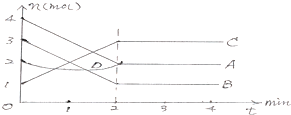

| A、该反应的方程式为:2A+2B?2C+D |
| B、该反应的方程式为:2A+2B=2C 催化剂是D |
| C、该反应是从正反应方向开始的 |
| D、平衡时,V(A)正=V(B)逆=V(C)逆 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、各物质的量的变化量之比等于系数是比;
B、催化剂在反应前后质量不会发生变化;
C、根据物质的量的变化来确定反应的方向;
D、根据化学反应的特征:正逆反应速率相等来回答.
B、催化剂在反应前后质量不会发生变化;
C、根据物质的量的变化来确定反应的方向;
D、根据化学反应的特征:正逆反应速率相等来回答.
解答:
解:A、A、B的量减小,C的量增大,所以A、B是反应物,C是产物,各物质的量的变化量之比,即为2:2:2,等于系数是比,D在反应前后质量不会发生变化,是催化剂,反应为:A+B?C,故A错误;
B、根据D在反应前后质量不会发生变化可以确定D是催化剂,该反应的方程式为:A+B?C,故B错误;
C、该反应中反应物和产物的初始量都不是零,可以是从正反应方向开始的,也可以是从逆方向开始的,故C错误;
D、根据化学反应的特征:正逆反应速率相等,所以平衡时,V(A)正=V(B)逆=V(C)逆,故D正确.
故选D.
B、根据D在反应前后质量不会发生变化可以确定D是催化剂,该反应的方程式为:A+B?C,故B错误;
C、该反应中反应物和产物的初始量都不是零,可以是从正反应方向开始的,也可以是从逆方向开始的,故C错误;
D、根据化学反应的特征:正逆反应速率相等,所以平衡时,V(A)正=V(B)逆=V(C)逆,故D正确.
故选D.
点评:本题考查学生化学方程式的书写以及平衡状态的建立和特征等方面的知识,属于综合知识的考查题,难度不大.

练习册系列答案
相关题目
 25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是( )
25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是( )| A、若B点的横坐标a=12.5,且有c(Na+)=c(CH3COO-) |
| B、对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C、D点时,c(CH3COO-)+c(CH3COOH)=c(Na+) |
| D、C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
近几年一种新型的甜味剂--木糖醇悄悄的走进人们的生活,因为木糖醇是一种理想的蔗糖代替品,它具有甜味足、溶解性好、防龋齿、适合糖尿病患者等优点.木糖醇是一种白色粉末状的固体,结构简式为:CH2OH(CHOH)3CH2OH.下列有关木糖醇的叙述错误的是( )
| A、木糖醇与葡萄糖、果糖等一样是一种单糖 |
| B、木糖醇极易溶于水 |
| C、木糖醇是一种五元醇 |
| D、木糖醇是一种无糖型植物甜味剂 |
下列关于常见有机物的说法中,不正确的是( )
| A、甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| B、乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的反应类型不同 |
| C、塑料、合成橡胶、合成纤维都属于合成有机高分子材料 |
| D、化学式均为(C6H10O5)n的淀粉和纤维素互为同分异构体 |
1mol某烷烃完全燃烧消耗的O2为1l mol,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有( )
| A、4种 | B、5种 | C、6种 | D、7种 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )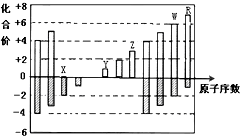

| A、原子半径:Z>Y>X |
| B、气态氢化物的稳定性:W>R |
C、X的一种氢化物具有氧化性,其电子式为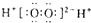 |
| D、Y和Z两者最高价氧化物对应的水化物能相互反应 |