题目内容
10.在一定温度下,可逆反应X(g)+3Y(g)?2Z(g)达到平衡的标志是( )①Z生成的速率与Z分解的速率相等
②单位时间生成a mol X,同时生成3a mol Y
③X、Y、Z的浓度不再变化
④X、Y、Z的分子数比为1:3:2
⑤X、Y、Z的浓度相等
⑥X、Y、Z的质量不再发生变化.
| A. | ①③⑥ | B. | ①②③ | C. | ①②⑤⑥ | D. | ①②③④⑤⑥ |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:①Z生成的速率与Z分解的速率相等,正逆反应速率相等,达平衡状态,故正确;
②单位时间生成a mol X,同时生成3a mol Y,都反映的是逆向,故错误;
③X、Y、Z的浓度不再变化,正逆反应速率相等,达平衡状态,故正确;
④当体系达平衡状态时,X、Y、Z的分子数比可能为1:3:2,也可能不是,与各物质的初始浓度及转化率有关,故错误;
⑤X、Y、Z的浓度不变,而不是相等,故错误;
⑥X、Y、Z的质量不再发生变化,正逆反应速率相等,达平衡状态,故正确;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
20.下列过程中△H小于零的是( )
| A. | 石灰石高温分解 | B. | 铝与盐酸的反应 | ||
| C. | 二氧化碳与碳反应 | D. | 氢氧化钡晶体与氯化铵反应 |
18.在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.5mol/L,用石墨作电极电解此溶液,当通电一段时间后,当阳极上收集到22.4L(标准状况)气体时,阴极才开始产生气体.则原溶液中K+的物质的量浓度为( )
| A. | 2.0 mol/L | B. | 1.5 mol/L | C. | 1.0 mol/L | D. | 0.5 mol/L |
15.下列有机物的命名及名称书写均正确的是( )
| A. | CH2BrCH2Br 二溴乙烷 | B. | CH3CH(NH2)CH2COOH 3-氨基丁酸 | ||
| C. | 硬酯酸甘油脂  | D. | 2,2-二甲基-3-丁醇 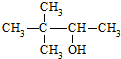 |
19.在实验室配制0.10mol•L-1的KOH溶液,下列操作会导致所配溶液浓度偏高的是( )
| A. | 转移溶液时使用的烧杯未洗涤 | |
| B. | 定容时仰视读取刻度线 | |
| C. | 原容量瓶洗净后有少量蒸馏水 | |
| D. | 固体溶解后立即转移到容量瓶内,定容 |
20.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 常温常压下,11.2 L甲烷中含有的氢原子数为2NA | |
| B. | 标准状况下,0.3 mol 二氧化硫中含有氧原子数为0.6NA | |
| C. | 4g金属钙变成钙离子时,失去电子数目为0.1NA | |
| D. | 常温下,1 L 0.1mol•L-1 MgCl2溶液中含有Mg2+数为0.1NA |

 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为 .
. .
.