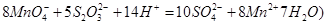题目内容
取10 g软锰矿(主要成分为MnO2)跟足量的浓盐酸在加热条件下充分反应,收集到氯气7.1 g。(1)写出反应的化学方程式;
(2)求该软锰矿中MnO2的质量分数;
(3)被氧化的HCl的物质的量。
解析:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
87 g 被氧化2 mol 71 g
m(MnO2) y 7.1 g
m(MnO2)=8.7 g y=0.2 mol
∴MnO2的质量分数为
![]()
∴被氧化的HCl为0.2 mol。
答案:(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)87% (3)0.2 mol

练习册系列答案
相关题目
 标准Na2S2O3溶液,需准确称取Na2S2O3固体的质量
标准Na2S2O3溶液,需准确称取Na2S2O3固体的质量 标准Na2S2O3溶液进行滴定,滴定至终点消耗Na2S2O3溶液12.00mL。计算该KMnO4产品的纯度。(有关离子方程式为:
标准Na2S2O3溶液进行滴定,滴定至终点消耗Na2S2O3溶液12.00mL。计算该KMnO4产品的纯度。(有关离子方程式为: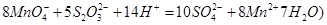
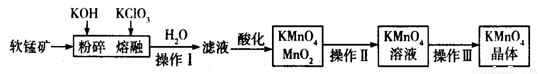
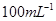 标准Na2S2O3溶液,需准确称取Na2S2O3固体的质量
标准Na2S2O3溶液,需准确称取Na2S2O3固体的质量 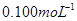 标准Na2S2O3溶液进行滴定,滴定至终点消耗Na2S2O3溶液12.00mL。计算该KMnO4产品的纯度。(有关离子方程式为:
标准Na2S2O3溶液进行滴定,滴定至终点消耗Na2S2O3溶液12.00mL。计算该KMnO4产品的纯度。(有关离子方程式为: