题目内容
以下实验能达到预期目的是( )
| A、相同条件下,测定Na2CO3、Na2SO4两溶液的pH,比较硫、碳的非金属性强弱 |
| B、向煮沸的1 mol?L-1的 NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
| C、向MgCl2、AlCl3溶液中通入NH3,比较镁、铝的金属性强弱 |
| D、称量2.5gCuSO4?5H2O晶体溶于100mL水配成0.10mol?L-1的硫酸铜溶液 |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律
专题:元素及其化合物
分析:A、先根据盐的pH判断对应酸的强弱,最高价含氧酸的酸性越强,则非金属性越强;
B、氢氧化钠与氯化铁反应生成沉淀;
C、氢氧化镁和氢氧化铝均不能溶于氨水;
D、水的体积不等于溶于的体积.
B、氢氧化钠与氯化铁反应生成沉淀;
C、氢氧化镁和氢氧化铝均不能溶于氨水;
D、水的体积不等于溶于的体积.
解答:
解:A、Na2CO3溶液显碱性,Na2SO4溶液显中性,则硫酸的酸性大于碳酸,最高价含氧酸的酸性越强,则非金属性越强,所以非金属性:S>C,故A正确;
B、氢氧化钠与氯化铁反应生成沉淀,不能生成胶体,向煮沸的蒸馏水中滴加FeCl3饱和溶液制备Fe(OH)3胶体,故B错误;
C、氢氧化镁和氢氧化铝均不能溶于氨水,则能向MgCl2、AlCl3溶液中通入NH3,均生成氢氧化铝沉淀,所以不能比较镁、铝的金属性强弱,故C错误;
D、水的体积不等于溶于的体积,称量2.5gCuSO4?5H2O晶体溶于100mL水配成溶液,则溶液的体积不能确定,所以溶液的浓度不能确定,故D错误.
故选A.
B、氢氧化钠与氯化铁反应生成沉淀,不能生成胶体,向煮沸的蒸馏水中滴加FeCl3饱和溶液制备Fe(OH)3胶体,故B错误;
C、氢氧化镁和氢氧化铝均不能溶于氨水,则能向MgCl2、AlCl3溶液中通入NH3,均生成氢氧化铝沉淀,所以不能比较镁、铝的金属性强弱,故C错误;
D、水的体积不等于溶于的体积,称量2.5gCuSO4?5H2O晶体溶于100mL水配成溶液,则溶液的体积不能确定,所以溶液的浓度不能确定,故D错误.
故选A.
点评:本题考查化学实验方案的评价,涉及非金属性和金属性的判断、胶体的制备、溶液的配制等,侧重于实验技能的考查,题目难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的数值,则下列说法正确的是( )
| A、2.24 L C4H6中含有碳碳叁键数一定为0.1×6.02×1023 |
| B、在标准状态下,11.2L NO与11.2L O2混合后气体分子数为0.75NA |
| C、106g Na2CO3固体中的阴离子数为NA |
| D、含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA |
 某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图,则下列说法中,正确的是(说明:一种小球代表一种元素的原子)( )
某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图,则下列说法中,正确的是(说明:一种小球代表一种元素的原子)( )| A、图中的反应物都是化合物 |
| B、该反应属于置换反应 |
| C、该反应属于复分解反应 |
| D、该反应不符合质量守恒定律 |
下列各组物质中,将前者加入后者时,无论前者是否过量,都能用一个化学方程式表示的是( )
| A、稀盐酸,碳酸钠溶液 |
| B、稀硫酸,偏铝酸钠溶液 |
| C、铜,氯化铁溶液 |
| D、浓氨水,硝酸银溶液 |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、24g镁单质变为镁离子时,失去的电子数为NA |
| B、48.3gNa2SO4?10H2O中所含水分子的数目为0.15NA个 |
| C、18g水中所含的电子数为NA |
| D、3.2g氧气所含氧原子数为0.2NA |
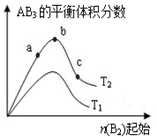 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图示可得出的判断结论正确的是( )
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图示可得出的判断结论正确的是( )| A、反应速率a>b>c |
| B、达到平衡时,A2的转化率大小为:b>a>c |
| C、若T2>T1,则正反应一定是放热反应 |
| D、达到平衡时,AB3的物质的量大小为:c>b>a |
下列有机物的命名正确的是( )
| A、2,3,4-三甲基庚烷 |
| B、2-甲基-4-乙基戊烷 |
| C、3-甲基丁烷 |
| D、2,3,3-三甲基丁烷 |
在一定量的偏铝酸钠溶液中,加入下列哪一种溶液可使获得的沉淀量最大( )
| A、Al2(SO4)3 |
| B、HCl |
| C、CO2 |
| D、H2SO4 |
有下列物品或设备:①计算机芯片 ②玻璃 ③水晶 ④石英钟表 ⑤玛瑙手镯⑥硅太阳能电池 ⑦光导纤维,所用材料为SiO2或要用到SiO2的是( )
| A、全部 | B、②③④⑤⑦ |
| C、①⑥ | D、①②⑦ |