题目内容
11.H2与D2的最确切关系是( )| A. | 同系物 | B. | 同位素 | ||
| C. | 同素异形体 | D. | 同种物质的不同分子 |
分析 A.结构相似组成上相差CH2的有机物为同系物;
B.质子数相同中子数不同的同种元素的不同原子互称同位素;
C.同种元素的同种原子组成的不同单质为同素异形体;
D.H2与D2原子结构中原子核外电子相同,质量数不同.
解答 解:H2与D2的构成是分子结构,属于氢气单质,不是有机化合物,不是原子,所以不属于同系物、同位素,H2与D2的分子式相同、结构相同,则为同一物质,最确切关系是同种物质的不同分子,故选D.
点评 本题考查了原子结构、核素、同位素、同素异形体等概念实质的理解应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列表示正确的是( )
| A. | HClO的结构式:H-O-Cl | B. | X=11,图表示钠原子的结构示意图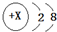 | ||
| C. | CCl4的电子式: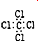 | D. | 乙炔的最简式:C2H2 |
2.下列有关实验的描述正确的是( )
| A. | Fe(OH)3胶体的制备:将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液.继续煮沸至溶液呈红褐色,停止加热 | |
| B. | 乙酸乙酯的制备:在一支试管中加入3mL浓硫酸,然后慢慢加入2mL无水乙醇和2mL无水乙酸,加入几粒沸石用酒精灯小火加热 | |
| C. | 碳酸钠溶液的焰色反应:用铂丝直接蘸取碳酸钠溶液,在外焰上灼烧,观察火焰颜色 | |
| D. | 在纯锌与稀H2SO4反应中滴入少量的Cu(NO3)2溶液后生成H2的反应速率加快 |
19.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 相同温度下,测定某物质的量浓度的H2SO4溶液,H3PO4溶液的pH | pH(H2SO4)溶液<pH(H3PO4)溶液 | 非金属性S>P |
| B | 将SO2通入紫色石蕊溶液中 | 溶液先变红后褪色 | SO2具有酸性、漂白性 |
| C | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+、NH3•H2O能大量共存 |
| D | 相同的铝片分别和同体积,同温度且c(H+)相等的盐酸,硫酸发生反应 | 为盐酸反应产生气体的速率快 | 酸性;盐酸>硫酸 |
| A. | A | B. | B | C. | C | D. | D |
6.二甲酸钾是一种白色晶体,商品名为弗米(Formil),是一种能替代抗生素的促生长剂,化学式为KH(HCOO)2,具有吸湿性,易溶于水.
二甲酸钾的生产工艺流程如下:
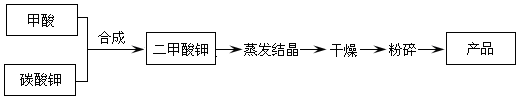
(1)以甲酸和碳酸钾为原料生产二甲酸钾,实验测得反应条件对产品回收率的影响如下:
表1 反应温度对产品回收率的影响
表2 反应物料比对产品回收率的影响
备注:表2中反应物料比为甲酸和无水碳酸钾的物质的量之比.
①写出甲酸和碳酸钾生产二甲酸钾的化学方程式:4HCOOH+K2CO3=2KH(HCOO)2+CO2↑+H2O.
②实际生产二甲酸钾时应选择的最佳反应条件是反应温度应控制在50℃∽60℃,反应物料比应选择4:1.由表1可知反应温度过高,反应回收率反而会降低,其原因可能是温度过高,甲酸易挥发.
(2)测定某弗米产品纯度的实验方法如下:
称取该弗米产品2.5g,将其全部溶解在水中,配制成250mL未知浓度的溶液,取出25.00mL于锥形瓶中,再滴加2~3滴指示剂,用0.10mol•L-1的NaOH溶液滴定至终点,消耗NaOH溶液的体积为18.50mL.
①加入的指示剂是酚酞(选填“甲基橙”、“石蕊”或“酚酞”),用NaOH溶液滴定至终点的现象是溶液由无色恰好变成浅红色且在半分钟内不褪色.
②上述弗米产品中二甲酸钾的质量分数为96.2%.
二甲酸钾的生产工艺流程如下:

(1)以甲酸和碳酸钾为原料生产二甲酸钾,实验测得反应条件对产品回收率的影响如下:
表1 反应温度对产品回收率的影响
| 反应温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 产品回收率(%) | 75.6 | 78.4 | 80.6 | 82.6 | 83.1 | 82.1 | 73.7 |
| 反应物料比 | 2:1 | 3:1 | 4:1 | 5:1 | 6:1 | 7:1 |
| 产品回收率(%) | 0 | 38.4 | 82. 6 | 83.6 | 84.5 | 84.8 |
①写出甲酸和碳酸钾生产二甲酸钾的化学方程式:4HCOOH+K2CO3=2KH(HCOO)2+CO2↑+H2O.
②实际生产二甲酸钾时应选择的最佳反应条件是反应温度应控制在50℃∽60℃,反应物料比应选择4:1.由表1可知反应温度过高,反应回收率反而会降低,其原因可能是温度过高,甲酸易挥发.
(2)测定某弗米产品纯度的实验方法如下:
称取该弗米产品2.5g,将其全部溶解在水中,配制成250mL未知浓度的溶液,取出25.00mL于锥形瓶中,再滴加2~3滴指示剂,用0.10mol•L-1的NaOH溶液滴定至终点,消耗NaOH溶液的体积为18.50mL.
①加入的指示剂是酚酞(选填“甲基橙”、“石蕊”或“酚酞”),用NaOH溶液滴定至终点的现象是溶液由无色恰好变成浅红色且在半分钟内不褪色.
②上述弗米产品中二甲酸钾的质量分数为96.2%.
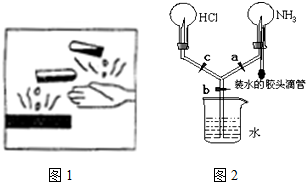
12.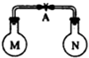 室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
 室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | H2 | NH3 | NO |
| 气体N | SO2 | Cl2 | HCl | O2 |
| A. | ②④①③ | B. | ①②③④ | C. | ④①②③ | D. | ①④③② |
10.下列叙述中正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | CH4、CCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的稳定性依次增强 | |
| D. | CS2、H2O、C2H2都是直线形分子 |