题目内容
16.下列说法正确的是( )| A. | HOCH2CH=CH2能发生取代反应,加成反应、氧化反应 | |
| B. | 月桂烯(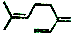 )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 | |
| C. | 甲烷、乙烯、苯和乙醇都能使酸性KMnO4溶液褪色 | |
| D. | 油脂皂化反应得到高级脂肪酸与甘油 |
分析 A.HOCH2CH=CH2中含-OH、碳碳双键,结合醇、烯烃的性质分析;
B. 中2个双键之间的C为四面体构型;
中2个双键之间的C为四面体构型;
C.甲烷、苯与高锰酸钾不反应;
D.油脂在碱性条件下的水解反应为皂化反应.
解答 解:A.HOCH2CH=CH2中含-OH可发生取代反应、氧化反应,含碳碳双键可发生加成反应、氧化反应,故A正确;
B. 中2个双键之间的C为四面体构型,则所有碳原子不一定共面,故B错误;
中2个双键之间的C为四面体构型,则所有碳原子不一定共面,故B错误;
C.甲烷、苯与高锰酸钾不反应,而乙烯、乙醇都能使酸性KMnO4溶液褪色,故C错误;
D.油脂在碱性条件下的水解反应为皂化反应,油脂皂化反应得到高级脂肪盐与甘油,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项B为解答的难点,题目难度不大.

练习册系列答案
相关题目
1.Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示.由图可知,当铁的浸出率为70%时,所采用的实验条件为100℃、2h或90℃、5h.

(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O.
(3)TiO2•xH2O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
分析40℃时TiO2•xH2O转化率最高的原因温度高反应速率加快,但温度过高过氧化氢分解、氨水易挥发,影响转化率.
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为4.
(5)若“滤液②”中c(Mg2+)=0.02mol•L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10-5,此时是否有Mg3(PO4)2沉淀生成?c(PO43-)=$\frac{1.3×1{0}^{22}}{1×1{0}^{-5}}$=1.0×10-17mol/L,Qc[Mg3(PO4)2]=($\frac{0.02mol/L}{2}$)3×(1.0×10-17mol/L)2=1.69×10-40<Ksp=1.0×10-24,则无沉淀生成(列式计算).FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式2FePO4+Li2CO3+H2C2O4$\frac{\underline{\;高温\;}}{\;}$2LiFePO4+H2O+3CO2↑.

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示.由图可知,当铁的浸出率为70%时,所采用的实验条件为100℃、2h或90℃、5h.

(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O.
(3)TiO2•xH2O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:
| 温度/℃ | 30 | 35 | 40 | 45 | 50 |
| TiO2•xH2O转化率/% | 92 | 95 | 97 | 93 | 88 |
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为4.
(5)若“滤液②”中c(Mg2+)=0.02mol•L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10-5,此时是否有Mg3(PO4)2沉淀生成?c(PO43-)=$\frac{1.3×1{0}^{22}}{1×1{0}^{-5}}$=1.0×10-17mol/L,Qc[Mg3(PO4)2]=($\frac{0.02mol/L}{2}$)3×(1.0×10-17mol/L)2=1.69×10-40<Ksp=1.0×10-24,则无沉淀生成(列式计算).FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式2FePO4+Li2CO3+H2C2O4$\frac{\underline{\;高温\;}}{\;}$2LiFePO4+H2O+3CO2↑.
4.下列说法正确的是( )
| A. | 煤的干馏和石油的分馏都是物理变化 | |
| B. | 1-氯丙烷和2-氯丙烷的消去产物相同 | |
| C. | 正戊烷、异戊烷、新戊烷的沸点逐渐升高 | |
| D. | 除去苯中苯酚,加入溴水后过滤 |
1.下列说法正确的是( )
| A. | 石油液化气的主要成份为甲烷 | |
| B. | 燃料的脱硫、脱氮都是减少酸雨产生的措施 | |
| C. | BaSO4难溶于水是弱电解质,在医学上用作钡餐 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
8.下列说法正确的是( )
| A. | 反应N2 (g)+3H2 (g)?2NH3 (g)的△H<0,△S>0 | |
| B. | 地下钢铁管道用导线连接锌块可以减缓管道的腐蚀 | |
| C. | 常温下,Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+ )≤5.6×10-4 mol•L-1 | |
| D. | 常温常压下,锌与稀H2SO4反应生成11.2 L H2,反应中转移的电子数为6.02×1023 |
10.下列反应中,在原理上可以设计成原电池的是( )
| A. | Ba(OH)2•8H2O与NH4Cl的反应 | B. | NaOH溶液与盐酸的反应 | ||
| C. | 甲烷与氧气的反应 | D. | 石灰石的分解反应 |
11.下列示意图与对应的化学反应关系不一致的是( )
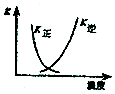 A.2SO2(g)+O2(g)?2SO3(g)△H<0 |  B.25℃时,用0.1mol/L盐酸滴定20mL0.1mol/LNaOH溶液 |
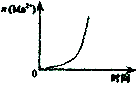 C.酸性KmnO4溶于与过量的H2C2O4溶液混合 |  D.CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0,使用催化剂(a)和未使用催化剂(b) |
| A. | A | B. | B | C. | C | D. | D |
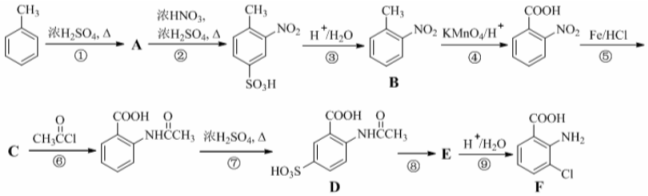

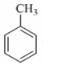 分子中不同化学环境的氢原子共有4种,共面原子数目最多为13.
分子中不同化学环境的氢原子共有4种,共面原子数目最多为13.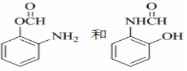 .
. ,该步反应的主要目的是保护氨基.
,该步反应的主要目的是保护氨基.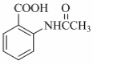 为主要原料,经最少步骤制备含肽键聚合物的流程.
为主要原料,经最少步骤制备含肽键聚合物的流程.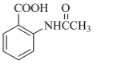 …$→_{反应条件}^{反应试剂}$目标化合物
…$→_{反应条件}^{反应试剂}$目标化合物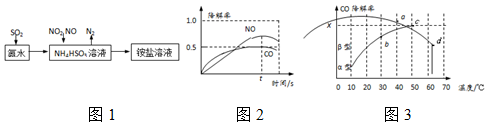
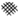 ”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围
”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围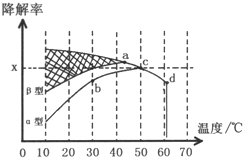 .
.